
分析 (1)根据m=nM计算;
(2)计算出NaHCO3和KHCO3的物质的量,根据反应HCO3-+H+=CO2↑+H2O计算盐酸的物质的量;
(3)碳酸氢盐与盐酸按1:1反应,盐酸过量,碳酸氢盐完全反应,根据碳元素守恒计算二氧化碳的体积;
(4)假定碳酸氢盐全是NaHCO3,或者全是KHCO3,根据碳元素守恒计算生成二氧化碳的物质的量,实际体积介于两种情况之间.
解答 解:(1)等物质的量的NaHCO3和KHCO3质量比为84g/mol:100g/mol=21:25,故答案为:21:25;
(2)n(NaHCO3)=n(KHCO3)=$\frac{ag}{84g/mol+100g/mol}$=$\frac{a}{184}$mol,混合物中n(HCO3-)=2×$\frac{a}{184}$mol=$\frac{a}{92}$mol,由HCO3-+H+=CO2↑+H2O,可知n(HCl)=n(H+)=n(HCO3-)=$\frac{a}{92}$mol,
故答案为:$\frac{a}{92}$mol;
(3)盐酸过量,NaHCO3和KHCO3组成的混合物完全反应,根据碳元素守恒可知,n(CO2)=n(NaHCO3)+(KHCO3)=$\frac{a}{92}$mol,所以标准状况下生成CO2的体积为=$\frac{a}{92}$mol×22.4L/mol=$\frac{22.4a}{92}$L,
故答案为:$\frac{22.4a}{92}$;
(4)假定碳酸氢盐全是NaHCO3,则n(NaHCO3)=$\frac{ag}{84g/mol}$=$\frac{a}{84}$mol,NaHCO3完全反应,根据碳元素守恒,可知生成二氧化碳n(CO2)=n(NaHCO3)=$\frac{a}{84}$mol,则V(CO2)=$\frac{22.4a}{84}$L,
假定碳酸氢盐全是KHCO3,则n(KHCO3)=$\frac{ag}{100g/mol}$=$\frac{a}{100}$mol,KHCO3完全反应,根据碳元素守恒,可知生成二氧化碳n(CO2)=n(KHCO3)=$\frac{a}{100}$mol,则V(CO2)=$\frac{22.4a}{100}$L,
故标况下$\frac{22.4a}{100}$L<V(CO2)<$\frac{22.4a}{84}$L,
故答案为:$\frac{22.4a}{100}$L<V(CO2)<$\frac{22.4a}{84}$L.
点评 本题考查混合物的计算,属于字母型计算,注意守恒思想与端值法在解题中应用,试题难度适中,培养了学生分析计算能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 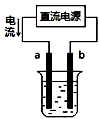 用装置精炼铜,则a极为粗铜,电解质溶液为CuSO4溶液 | |
| B. | 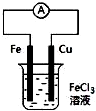 装置的总反应是:Cu+2Fe3+═Cu2++2Fe2+ | |
| C. | 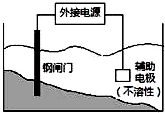 装置中钢闸门应与外接电源的负极相连 | |
| D. | 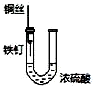 装置中的发生的是铁钉的析氢腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 每个分子中都含有氮分子 | B. | 每个分子中的氮原子个数相等 | ||
| C. | 每种物质中氮元素的质量分数相同 | D. | 都属于氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硅是生产光纤制品的基本原料 | |
| B. | 水玻璃可用于生产黏合剂和防火剂 | |
| C. | D${\;}_{2}^{16}$O中,质量数之和是质子数之和的两倍 | |
| D. | 石油分馏可获得乙烯、丙烯和丁二烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去N2中的少量O2:通过灼热的铜网,收集气体 | |
| B. | 除 CO2中的少量HCl:通入饱和Na2CO3溶液,收集气体 | |
| C. | 除去FeCl3溶液中的少量FeCl2:加入足量铁屑,充分反应后过滤 | |
| D. | 除去NaCl溶液中的少量AlCl3:加入适量氨水,过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 饱和氯水中 Cl-、NO3-、Na+、SO32- | |
| B. | pH=12的溶液中 NO3-、I-、Na+ | |
| C. | NaHS溶液中 SO42-、K+、Cl-、Al3+ | |
| D. | 使甲基橙变红的溶液中 C6H5O-、K+、SO42-、Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “绿色化学”的理念是从源头上减少和消除工业产生对环境的污染 | |
| B. | 氢能是清洁能源,工业上电解水法制大量氢气符合节能减排理念 | |
| C. | 如将纳米材料分散到液体分散剂中,该分散系可发生丁达尔现象,由此可推测纳米材料的直径为1~100nm之间 | |
| D. | 将苦卤浓缩、氧化,鼓入热空气或水蒸气提取海水中的溴 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com