
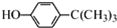
 工业用途广泛,可用于生产油溶性酚醛树脂、稳定剂和香料等.实验室以苯酚、叔丁基氯(CH3)3CCl等为原料制备对叔丁基苯酚.实验步骤如下:
工业用途广泛,可用于生产油溶性酚醛树脂、稳定剂和香料等.实验室以苯酚、叔丁基氯(CH3)3CCl等为原料制备对叔丁基苯酚.实验步骤如下: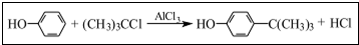 .该反应为放热反应,且实验的产率通常较低,可能的原因是由于叔丁基氯挥发导致产率降低.
.该反应为放热反应,且实验的产率通常较低,可能的原因是由于叔丁基氯挥发导致产率降低.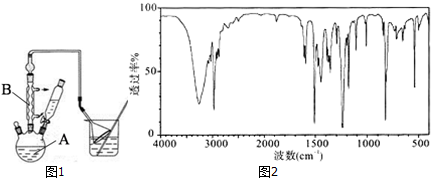
分析 (1)根据仪器的构造特点,可知仪器A是三颈烧瓶,仪器B是球形冷凝管;
(2)向A中加入少量无水AlCl3固体作催化剂,打开滴液漏斗旋塞,迅速有气体放,这说明苯环上的氢原子被取代,同时生成氯化氢,即产生的气体是氯化氢;
该反应为放热反应,反应过于激烈,放出大量热,因此导致体系温度升高,从而使得叔丁基氯挥发;
(3)氯化氢极易溶于水,则图中倒扣漏斗的作用是防止倒吸;
苯酚不溶于水,易溶在酒精中,若苯酚溶液沾到皮肤上可用酒精洗涤;
(4)苯酚的熔点较低且有毒,稍微加热固体即可转化为液体.因此用石油醚重结晶提纯粗产物的操作为将粗产物加到烧杯中,加入适量石油醚,加热使粗产品溶解,随后趁热过滤,将滤液静置,冷却结晶,滤出晶体;
(5)根据谱图的特征可知该谱图是红外光谱图;
(6)容量瓶、滴定管、分液漏斗在使用前均需要查漏;
(7)根据苯酚质量计算理论上可以生成对叔丁基苯酚的质量,进而计算产率.
解答 解:(1)根据仪器的构造特点可判断,仪器A是三颈烧瓶,仪器B是球形冷凝管,故答案为:三颈烧瓶;球形冷凝管;
(2)向A中加入少量无水AlCl3固体作催化剂,打开滴液漏斗旋塞,迅速有气体放,这说明苯环上的氢原子被取代,同时生成氯化氢,即产生的气体是氯化氢,因此出步骤2中发生主要反应的化学方程式为 .该反应为放热反应,反应过于激烈,放出大量热,因此导致体系温度升高,从而使得叔丁基氯挥发,因此导致产率降低,
.该反应为放热反应,反应过于激烈,放出大量热,因此导致体系温度升高,从而使得叔丁基氯挥发,因此导致产率降低,
故答案为: ;由于叔丁基氯挥发导致产率降低;
;由于叔丁基氯挥发导致产率降低;
(3)氯化氢极易溶于水,则图中倒扣漏斗的作用是防止倒吸.苯酚不溶于水,易溶在酒精中,若苯酚溶液沾到皮肤上可用酒精洗涤,
故答案为:防止倒吸;酒精;
(4)苯酚的熔点较低且有毒,稍微加热固体即可转化为液体.因此用石油醚重结晶提纯粗产物的操作为:将粗产物加到烧杯中,加入适量石油醚,加热使粗产品溶解,随后趁热过滤,将滤液静置,冷却结晶,滤出晶体,
故答案为:将粗产物加到烧杯中,加入适量石油醚,加热使粗产品溶解,随后趁热过滤,将滤液静置,冷却结晶,滤出晶体;
(5)根据谱图的特征可知该谱图是红外光谱图,故选:B;
(6)容量瓶、滴定管、分液漏斗在使用前均需要查漏,故选:BCD;
(7)1.6g苯酚理论上可以生成对叔丁基苯酚的质量是1.6g÷94g/mol×150g/mol=2.55g,所以对叔丁基苯酚的产率为$\frac{1.8g}{2.55g}$×100%=70.5%,
故答案为:70.5%.
点评 本题考查有机物制备实验方案设计与探究,涉及化学仪器、对装置与原理的分析与评价、实验安全、有机物结构式确定、物质的分离与提纯等,题目综合性较强,是对学生综合能力考查,有利于培养学生分析能力、实验能力、知识迁移应用能力.


 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | m+n<p | B. | 平衡向逆反应方向移动 | ||
| C. | C的体积分数增大 | D. | A的转化率降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 操作和现象 | 结论 | |
| A | 向装有Fe(NO3)2溶液的试管中加入稀H2SO4,在管口观察到红棕色气体 | HNO3分解生成了NO2 |
| B | 向淀粉溶液中加入稀H2SO4,加热几分钟,冷却后再加入新制Cu(OH)2浊液,加热,没有红色沉淀生成 | 淀粉没有水解成葡萄糖 |
| C | 向饱和Na2CO3溶液中通入足量CO2,溶液变浑浊 | 析出了NaHCO3 |
| D | 向无水乙醇中加入浓H2SO4,加热至170℃产生的气体通入酸性KMnO4溶液,红色褪去 | 使溶液褪色的气体是乙烯 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蛋白质、淀粉和油脂都属于高分子化合物 | |
| B. | 人造纤维.合成纤维.碳纤维.光导纤维主要成分都是纤维素 | |
| C. | 误食重金属盐类时,可以喝大量牛奶、蛋清或豆浆解毒 | |
| D. | 福尔马林主要成分是甲酸,由于可使蛋白质变性,可用于保存动物标本 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.24LNH3和CH4的混合气体,所含电子总数为2NA | |
| B. | 1mol乙醇(CH3CH2OH)分子中含有共价键总数为8NA | |
| C. | 1mol/LNa2CO3溶液中,含有CO32-离子数为NA | |
| D. | 6.4gCu与足量浓硝酸反应,用排水法收集的气体分子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在反应KC1O3+6HCl(浓)═KC1+3C12↑+3H2O中,每生成3 mol Cl2转移的电子数为NA | |
| B. | 1 mol K2S固体中含有3 NA个离子 | |
| C. | 1 mol 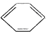 分子中含碳碳双键数为3 NA 分子中含碳碳双键数为3 NA | |
| D. | 含有NA个氖原子的氖气在标准状况下的体积约为11.2 L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com