
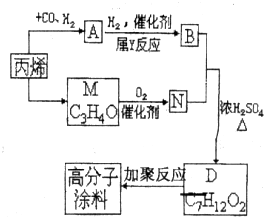
 有一种广泛用于汽车、家电产品上的高分子涂料,是按下列流程生产的.图中的(C3H4O)和A都可以发生银镜反应,N和M的分子中碳原子数相等,A的烃基上一氯取代位置有三种.
有一种广泛用于汽车、家电产品上的高分子涂料,是按下列流程生产的.图中的(C3H4O)和A都可以发生银镜反应,N和M的分子中碳原子数相等,A的烃基上一氯取代位置有三种.| 2×3+2-4 |
| 2 |
| 2×3+2-4 |
| 2 |
| 浓硫酸 |
| △ |
| 浓硫酸 |
| △ |
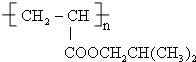 ,D在一定条件下发生加聚反应的化学方程式为nCH2=CH-COOCH2CH2CH2CH3
,D在一定条件下发生加聚反应的化学方程式为nCH2=CH-COOCH2CH2CH2CH3| 一定条件 |
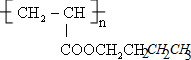 ,
,| 一定条件 |
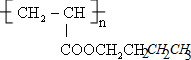 ;
;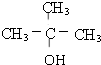 ,故答案为:
,故答案为: .
.


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
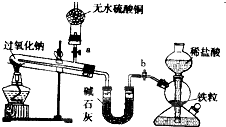 Na2O2是中学化学常用的强氧化剂,除了能与CO2、H2O反应外,还可与其他还原剂如H2、C发生反应,某化学课外兴趣小组为探究Na2O2与H2的反应情况下,设计了如图所示装置进行有关实验.
Na2O2是中学化学常用的强氧化剂,除了能与CO2、H2O反应外,还可与其他还原剂如H2、C发生反应,某化学课外兴趣小组为探究Na2O2与H2的反应情况下,设计了如图所示装置进行有关实验.查看答案和解析>>
科目:高中化学 来源: 题型:
| 化合物 | A | B | C |
| 结构简式 |  | 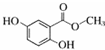 | 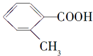 |
| 化合物 | D | E | F |
| 结构简式 | 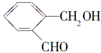 | 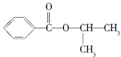 | 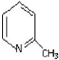 |


查看答案和解析>>
科目:高中化学 来源: 题型:
| 起始n(M):n(H2O) | M转化率 | H2O转化率 |
| 1:1 | 0.5 | 0.5 |
| 1:2 | 0.67 | 0.33 |
| 1:3 | 0.75 | 0.25 |

查看答案和解析>>
科目:高中化学 来源: 题型:
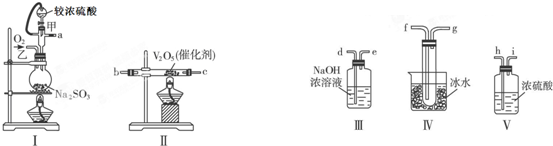
查看答案和解析>>
科目:高中化学 来源: 题型:
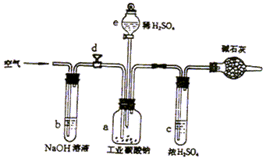 工业纯碱主要成份是无水碳酸钠,其中还含少量氯化钠,为测定工业纯碱中碳酸钠的质量分数:某学生设计了如图的装置:
工业纯碱主要成份是无水碳酸钠,其中还含少量氯化钠,为测定工业纯碱中碳酸钠的质量分数:某学生设计了如图的装置:查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D | |
| 与溴水混合的试剂 | 酒精 | 己烯 | 己烷 | 四氯化碳 |
| 现象 | 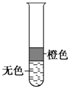 | 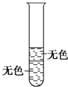 | 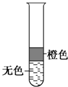 | 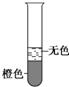 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com