
| A. | 乙醇 | B. | 盐酸 | C. | 一氧化碳 | D. | 硝酸 |
分析 铜丝灼烧成黑色.是生成了CuO:2Cu+O2$\frac{\underline{\;加热\;}}{\;}$2CuO,再结合CuO与选项中的物质发生的化学反应来分析判断.
解答 解:A、铜丝灼烧成黑色,立即放入乙醇中,CuO与乙醇反应:CuO+C2H5OH$\stackrel{△}{→}$CH3CHO+Cu+H2O,反应前后其质量不变,故A正确;
B、铜丝灼烧成黑色,立即放入盐酸中,CuO与盐酸反应,生成铜盐,质量减少,故B错误;
C、铜丝灼烧成黑色,立即放入一氧化碳中,氧化铜和一氧化碳发生氧化还原反应,生成二氧化碳和铜,铜的总质量不变,故C正确;
D、铜丝灼烧成黑色,立即放入硝酸中,CuO与硝反应,生成铜盐,质量减少,故D错误;
故选AC.
点评 本题主要考查了铜及其化合物的性质,难度不大,要注重过程的分析.


科目:高中化学 来源: 题型:解答题
 卤素的单质及其化合物在生产、生活中应用广泛.
卤素的单质及其化合物在生产、生活中应用广泛. (如${\;}_{1}^{2}$H).
(如${\;}_{1}^{2}$H).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯 | B. | 乙炔 | C. | 丙烯 | D. | 丙炔 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④⑤⑧⑨ | B. | ①③⑥⑦⑨ | C. | ①③⑤⑥⑦ | D. | ①②③⑤⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 凡是卤代烃一定能发生消去反应 | |
| B. | 一定条件下,Cl2可在甲苯的苯环或侧链上发生取代反应 | |
| C. | 苯不能使KMnO4溶液褪色,因此苯不能发生氧化反应 | |
| D. | 苯酚钠溶液中通入CO2生成苯酚,则碳酸的酸性比苯酚弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 重铬酸钾又名红矾钾,是化学实验室中的一种重要分析试剂.工业上以铬酸钾(K2CrO4)为原料,采用电化学法制备重铬酸钾(K2Cr2O7).制备装置如图所示(阳离子交换膜只允许阳离子透过). 制备原理:2CrO42-(黄色)+H+?Cr2O72-(橙色)+H2O.下列说法正确的是( )
重铬酸钾又名红矾钾,是化学实验室中的一种重要分析试剂.工业上以铬酸钾(K2CrO4)为原料,采用电化学法制备重铬酸钾(K2Cr2O7).制备装置如图所示(阳离子交换膜只允许阳离子透过). 制备原理:2CrO42-(黄色)+H+?Cr2O72-(橙色)+H2O.下列说法正确的是( )| A. | 电解时惰性电极应与直流电源的负极相连 | |
| B. | 通电后阴极室产生的现象为:产生无色气体,溶液由无色变黄色 | |
| C. | 制备过程中总的离子方程式为:2CrO42-+3H2O=Cr2O72-+2OH-+2H2↑+O2↑ | |
| D. | 若实验开始时在右室中加入38.8克的K2CrO4,tmin后测得右室中K与Cr的物质的量之比为3:2,此时电路中转移电子的物质的量为0.1mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
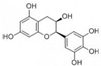
| A. | 分子中所有的原子共面 | |
| B. | 1mol EGC与4mol NaOH恰好完全反应 | |
| C. | 易发生氧化反应和取代反应,一定条件下可发生加成反应 | |
| D. | 易发生水解反应和显色反应,一定条件下可发生消去反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com