
【题目】某温度T1时,向容积为2L的恒容密闭容器中充入一定量的H2和I2(g),发生反应:H2(g)+I2(g) ![]() 2HI(g),反应过程中测定的部分数据见下表(表中t2>t1)。下列说法正确的是
2HI(g),反应过程中测定的部分数据见下表(表中t2>t1)。下列说法正确的是
反应时间/min | n(H2)/mol | n(I2)/mol |
0 | 0.9 | 0.3 |
t1 | 0.8 | |
t2 | 0.2 |
A. 反应在tmin内的平均速率为:v(H2)=![]() mol-1·L-1·min-l
mol-1·L-1·min-l
B. 保持其他条件不变,向平衡体系中再通0.20molH2,与原平衡相比,达到新平衡时I2(g)转化率增大,H2的体积分数不变
C. 保持其他条件不变,起始时向容器中充入的H2和I2(g)都为0.5mol,达到平衡时 n(HI)=0.2mol
D. 升高温度至T2时,上述反应平衡常数为0.18,则正反应为吸热反应
【答案】C
【解析】A.根据v=![]() 进行计算;B.恒温恒压,增加一种反应物浓度可以提高另一种反应物的转化率,自身的体积分数增大;C.平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积,结合平衡三段式计算平衡常数,再根据平衡常数计算平衡时HI的物质的量;D.平衡常数减小,平衡逆向移动,依此进行判断。
进行计算;B.恒温恒压,增加一种反应物浓度可以提高另一种反应物的转化率,自身的体积分数增大;C.平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积,结合平衡三段式计算平衡常数,再根据平衡常数计算平衡时HI的物质的量;D.平衡常数减小,平衡逆向移动,依此进行判断。
A.由表中数据可知,t1min内参加反应的H2的物质的量为0.9mol-0.8mol=0.1mol,故v(H2)=![]() =
=![]() =
=![]() mol/(Lmin),故A错误;
mol/(Lmin),故A错误;
B.保持其他条件不变,向平衡体系中再通入0.20molH2,与原平衡相比,H2的体积分数增大;H2的浓度增大,平衡正向移动,故I2(g)转化率增大,故B错误;
C.t1时, H2(g) + I2(g)2HI(g)
起始(mol) 0.9 0.3 0
转化(mol) 0.1 0.1 0.2
平衡(mol) 0.8 0.2 0.2
平衡常数K=![]() =
=![]() =0.25,
=0.25,
t2时, H2(g)+I2(g)2HI(g)
起始(mol) 0.5 0.5 0
转化(mol) x x 2x
平衡(mol)0.5-x 0.5-x 2x
K=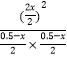 =0.25,解得x=0.1mol,故平衡时n(HI)=0.1mol×2=0.2mol,故C正确;
=0.25,解得x=0.1mol,故平衡时n(HI)=0.1mol×2=0.2mol,故C正确;
D.升高温度至T2时,上述反应平衡常数为0.18<0.25,说明升高温度,平衡逆向移动,故正反应为放热反应,故D错误;故选C。


 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源: 题型:
【题目】化合物A的相对分子质量为136,分子式为C8H8O2。A分子中只含一个苯环且苯环上只有一个取代基,其红外光谱和核磁共振氢谱如下图。下列关于A的说法中不正确的是

A. 与A属于同类化合物的同分异构体只有4种
B. 符合题中A分子结构特征的有机物只有1种
C. A在一定条件下可与3 molH2发生加成反应
D. A分子属于酯类化合物,在一定条件下能发生水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某原电池装置如图所示。下列说法错误的是

A. 铜电极上发生氧化反应
B. 在外电路中,电流由银电极流向铜电极
C. 当0.1 mol Cu完全溶解时,流经电解质溶液的电子数目为0.2NA
D. 将铜片浸入AgNO3溶液中发生的化学反应与该原电池反应相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式的书写及评价均合理的是( )
选项 | 离子方程式 | 评价 |
A | 将2 mol Cl2通入含1 mol FeI2的溶液中: 2Fe2++2I-+2Cl2===2Fe3++4Cl-+I2 | 正确;Cl2过量,可将Fe2+、I-均氧化 |
B | Ba(HCO3)2溶液与足量的NaOH溶液反应: Ba2++HCO3-+OH-===BaCO3↓+H2O | 正确;酸式盐与碱反应生成正盐和水 |
C | 过量SO2通入NaClO溶液中: SO2+H2O+ClO-===HClO+HSO3- | 正确;说明酸性:H2SO3强于HClO |
D | 1 mol/L的NaAlO2溶液和2.5 mol/L的HCl溶液等体积混合: 2AlO2-+5H+===Al3++Al(OH)3↓+H2O | 正确;第一步反应和第二步反应消耗的H+的物质的量之比为2∶3 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生物燃料电池(BFC)是一种真正意义上的绿色电池,其工作原理如图所示。下列说法中不正确的是

A. C2极为电池正极
B. C1极的电极反应式为:C2H5OH+3H2O-12e-=2CO2+12H+
C. 电子由C2极经外电路导线流向C1极
D. 稀硫酸中的H+向C2极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在①丙烯(CH3—CH=CH2)、②氯乙烯、③苯、④乙醇四种有机化合物中,分子内所有原子均在同一平面的是( )
A. ①② B. ②③
C. ③④ D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图甲中①②③④表示不同化学元素所组成的化合物,图乙表示由四个单体构成的化合物。以下说法不正确的是( )

A. 若图甲中的②大量存在于皮下和内脏器官周围等部位,则②是脂肪
B. 若图甲中④能吸收、传递和转换光能,则④可用无水乙醇提取
C. 图乙中若单体是氨基酸,则该化合物彻底水解后的产物中氧原子数增加3个
D. 图乙中若单体是四种脱氧核苷酸,则该化合物彻底水解后的产物有5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】次硫酸氢钠甲醛(NaHSO2HCHO2H2O)俗称吊白块,在印染、医药以及原子能工业中有广 泛应用。以 Na2SO3、SO2、HCHO和锌粉为原料制备次硫酸氢钠甲醛的实验步骤如下: 已知:次硫酸氢钠甲醛易溶于水,微溶于乙醇,具有强还原性,且在 120℃以上发生分解。
步骤 1:在三颈烧瓶中加入一定量 Na2SO3 和水,搅拌溶解,缓慢通入 SO2,至溶液 pH 约为 4,制得 NaHSO3溶液。
步骤 2:将装置 A 中导气管换成橡皮塞。向烧瓶中加入稍过量的锌粉和一定量甲醛溶液,在 80~90℃下, 反应约 3h,冷却至室温,抽滤;

步骤 3:将滤液真空蒸发浓缩,冷却结晶。
(1)装置 B的烧杯中应加入的溶液是_________;冷凝管中冷却水从_______填“a”或“b”)口进水。
(2)A 中多孔球泡的作用是________。
(3)冷凝管中回流的主要物质除 H2O 外还有________(填化学式)。
(4)写出步骤 2 中发生反应的化学方程式________。
(5)步骤 3 中在真空容器中蒸发浓缩的原因是________。
(6)为了测定产品的纯度,准确称取 2.0g 样品,完全溶于水配成 100mL 溶液,取 20.00mL 所配溶液, 加入过量碘完全反应后(已知 I2 不能氧化甲醛,杂质不反应),加入 BaCl2 溶液至沉淀完全,过滤、洗涤、 干燥至恒重得到白色固体 0.466g,则所制得的产品的纯度为________ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com