
| A、盐酸和氢氧化钠溶液反应 | B、氯化氢气体溶解于水 | C、氯化氢气体遇到氨气产生“白烟” | D、锌片投入稀硫酸中产生气体 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:




查看答案和解析>>
科目:高中化学 来源: 题型:








 I2+Z+H2O,其中的R元素.
I2+Z+H2O,其中的R元素.查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素编号 | 元素性质与原子(或分子)结构 |
| T | 最外层电子数是次外层电子数的3倍 |
| X | 常温下单质为双原子分子,分子中含有3对共用电子对 |
| Y | M层比K层少1个电子 |
| Z | 第3周期元素的简单离子中半径最小 |
查看答案和解析>>
科目:高中化学 来源:学习周报 化学 人教课标高二版(选修4) 2009-2010学年 第8期 总第164期 人教课标版(选修4) 题型:013
|
下列关于弱电解质的说法,正确的是 | |
| [ ] | |
A. |
弱电解质需要通电才能发生电离 |
B. |
醋酸达到电离平衡时,不存在反应: CH3COO-+H+ |
C. |
H2SO4是共价化合物,所以它是弱电解质 |
D. |
弱电解质溶液中,既有溶质分子,又有溶质电离产生的离子 |
查看答案和解析>>
科目:高中化学 来源:2015届山东省济宁市高一2月月考化学试卷(解析版) 题型:填空题
(13分)试根据下表填空:
A
B C D E F
G H I J L K M
N Q
(1)请写出元素Q的基态原子电子排布式 ;元素N在周期表中的位置 周期 族。
(2)基态D原子核外有 个未成对电子;D2分子中分别有 个, 个π键。
(3)化合物DA5中既含离子键,又含共价键和配位键,请写出它的电子式 。
(4)表四中的元素能形成XY2型的共价分子有CE2、CL2、BK2、LE2四种,其分子的空间构型中有一种与其他三种不同,它是 (填化学式);而形成XY3型的共价分子也有四种,它们分别是DA3、DF3、DK3、LE3,其分子的空间构型中也有一种与其他三种不同,它是 (填化学式),它是由_ 键(填“极性”或“非极性”,下同)构成的 分子。
(5)第三周期8种元素按单质熔点高低的顺序如右图所示,其中序号“8”所代表的元素是 (填元素符号);其中气态氢化物稳定性最强的元素是 (填下图中的序号)。

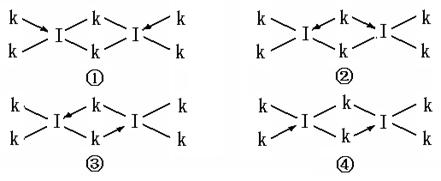
(6)科学家证实,IK3属于共价化合物,分子式为I2K6,其结构式为下列四种中的一种,你认为正确的结构式是____________。
(7)向Q的硫酸盐溶液中加入足量的DA3的水溶液过程中,请写出发生反应的离子方程式 ;最后生成配离子的结构式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com