
下列关于pH=12的Na2CO3溶液说法正确的是
A.升高溶液温度,溶液pH增大
B.c(Na+) +c(H+)=c(CO32-)+ c(HCO3-)+ c(OH-)
C.溶液中c(OH-)>c(HCO3-)> c(H+)
D.2c(Na+)=c(CO32-)+ c(HCO3-)+ c(H2CO3)
AC
【解析】
试题分析:碳酸钠是强碱弱酸盐,少部分碳酸根离子能够水解,即CO32—+H2O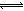 HCO3—+OH—,该水解反应是吸热反应,升高温度,促进碳酸根离子水解,氢氧根离子浓度增大,溶液的pH增大,故A选项正确;B项,违反电荷守恒原理,碳酸钠溶液中存在Na+、H+、CO32-、HCO3-、OH-,由于溶液呈电中性,则阳离子的正电荷总浓度等于阴离子的负电荷总浓度,即c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-),故B选项错误;碳酸根离子的水解分两步进行,CO32—+H2O
HCO3—+OH—,该水解反应是吸热反应,升高温度,促进碳酸根离子水解,氢氧根离子浓度增大,溶液的pH增大,故A选项正确;B项,违反电荷守恒原理,碳酸钠溶液中存在Na+、H+、CO32-、HCO3-、OH-,由于溶液呈电中性,则阳离子的正电荷总浓度等于阴离子的负电荷总浓度,即c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-),故B选项错误;碳酸根离子的水解分两步进行,CO32—+H2O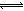 HCO3—+OH—,HCO3—+H2O
HCO3—+OH—,HCO3—+H2O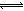 H2CO3+OH—,第一步水解程度大于第二步水解,碳酸钠溶液呈碱性,则溶液中c(OH-)>c(HCO3-)> c(H+),故C选项正确;D项,违反物料守恒原理,因为碳酸钠中钠离子是碳酸根离子的2倍,则平衡时溶液中c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3),故D选项错误。
H2CO3+OH—,第一步水解程度大于第二步水解,碳酸钠溶液呈碱性,则溶液中c(OH-)>c(HCO3-)> c(H+),故C选项正确;D项,违反物料守恒原理,因为碳酸钠中钠离子是碳酸根离子的2倍,则平衡时溶液中c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3),故D选项错误。
考点:考查水溶液中粒子浓度大小关系,涉及酸与盐溶液中电荷守恒关系式、溶液pH、水的离子积、电离平衡移动、溶液的酸碱性、盐与盐溶液中物料守恒关系式等。


科目:高中化学 来源:2010年宁波市八校高二下学期期末联考化学试题 题型:选择题
常温下,下列关于pH值的说法正确的是
A.在pH=12的溶液中,由水提供的c(OH-)一定是10-12mol/L。
B.把pH=2与pH=12的酸、碱溶液等体积混合后,所得溶液的pH值为7
C.pH=6与pH=4的两盐酸等体和混合后,所得溶液中c(H+)最接近0.5×(10-8+
10-10)mol/L
D.在稀氨水里加入NH4Cl晶体后,pH值会降低,若再向此溶液中加入少量稀盐酸或少量氢氧化钠溶液后,溶液的pH值都几乎不变
查看答案和解析>>
科目:高中化学 来源:2009-2010学年浙江省宁波市八校高二(下)期末化学试卷(解析版) 题型:选择题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com