
 2Ni(OH)2。据此反应式判断,下列叙述中正确的是
2Ni(OH)2。据此反应式判断,下列叙述中正确的是| A.电池放电时,H2是正极 |
| B.电池充电时,镍元素被还原 |
| C.充电时,电池负极的电极反应式为2H2O+2e—=H2+2OH— |
| D.电池放电时,H2是负极,负极周围溶液的pH不断增大 |
科目:高中化学 来源:不详 题型:单选题
 LiFePO4,负极:Li-e-
LiFePO4,负极:Li-e- Li+。下列说法中正确的是( )
Li+。下列说法中正确的是( )| A.充电时动力电池上标注“+”的电极应与外接电源的正极相连 |
B.放电时电池反应为FePO4+Li++e- LiFePO4 LiFePO4 |
| C.放电时电池内部Li+向负极移动 |
| D.放电时,在正极上Li+得电子被还原 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.原电池是将化学能转化为电能的装置 |
| B.轮船底部镶嵌锌块,锌作负极,以防船体被腐蚀 |
| C.钢铁腐蚀的负极反应:Fe-3e-=Fe3+ |
| D.电镀时,镀层金属作阳极,镀件作阴极 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.断开开关S1,闭合开关S2,化学能转化为电能,电能转化为光能等 |
| B.断开开关S1,闭合开关S2,此时构成的装置属于电解池 |
| C.断开开关S2,闭合开关S1,此时构成的装置属于原电池 |
| D.断开开关S2,闭合开关S1,化学能转化为电能 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
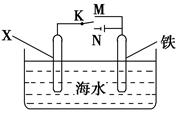
| A.铁被腐蚀过程实质是金属铁发生了还原反应 |
| B.若X为锌片,开关K置于M处,可减缓铁的腐蚀 |
| C.若X为碳棒,开关K置于M处,可减缓铁的腐蚀 |
| D.当K置于N处时,可减缓铁的腐蚀 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
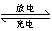 Fe(OH)2 + Ni(OH)2。
Fe(OH)2 + Ni(OH)2。| A.NiO2 | B.Fe | C.Fe(OH)2 | D.Ni(OH)2 |
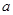 g M,则金属M的相对原子质量为 (用含“
g M,则金属M的相对原子质量为 (用含“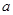 、x”的表达式表示)。
、x”的表达式表示)。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
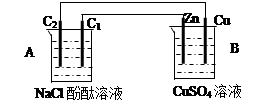
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用导线将铁片和铜片连接后,放入一盛有稀 H2SO4溶液的烧杯中 |
| B.将铁片直接放入一盛有稀 H2SO4溶液的烧杯中 |
| C.Cu片作阳极,铁片作阴极,电解一定量的H2SO4溶液 |
| D.Cu片作阴极,铁片作阳极,电解一定量的H2SO4溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com