


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
 我国在反兴奋剂问题上的立场是坚决支持“人文奥运”的.某种兴奋剂的结构如图所示.关于它的叙述正确的是( )
我国在反兴奋剂问题上的立场是坚决支持“人文奥运”的.某种兴奋剂的结构如图所示.关于它的叙述正确的是( )| A、它的分子式为C20H22O3 |
| B、它易溶于水 |
| C、它的分子中共平面的碳原子最多有16个 |
| D、1mol它最多可与7molH2和含4mol Br2的溴水发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用托盘天平称取11.7 g CuO粉末 |
| B、用广泛的pH试纸测得溶液的pH为6.2 |
| C、温度计显示的室温读数为25.69℃ |
| D、用100 mL量筒量取5.6 mL的稀硝酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
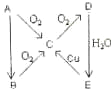 A、B、C、D、E、在一定条件下的转换条件如图所示:
A、B、C、D、E、在一定条件下的转换条件如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
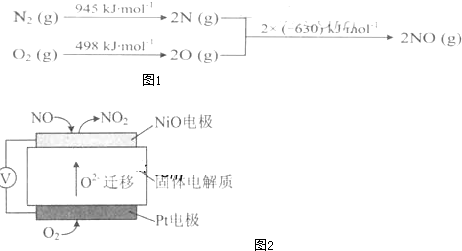
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在C(HCO3-)=0.1mol/L的溶液中NH4+、Al3+、Cl-、NO3- |
| B、在由水电离出的C(H+)=1×10-12mol/L的溶液中AlO2-、HCO3-、Na+、SO42- |
| C、在使红色石蕊试纸变蓝的溶液中SO32-、CO32-、Na+、K+ |
| D、pH=1的溶液中Mg2+、Fe2+、NO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
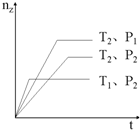 反应aX(g)+bY(g)cZ(g),在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量(nz)与反应时间(t)的关系如图所示.下列判断正确的是( )
反应aX(g)+bY(g)cZ(g),在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量(nz)与反应时间(t)的关系如图所示.下列判断正确的是( )| A、T1<T2,P1<P2,a+b<c正反应是吸热反应 |
| B、T1<T2,P1>P2,a+b<c正反应是吸热反应 |
| C、T1>T2,P1>P2,a+b>c逆反应是吸热反应 |
| D、T1>T2,P1<P2,a+b>c逆反应是吸热反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com