
| A.该电池的正极是Zn,负极是Ag2O |
| B.该电池负极的电极反应式为:Zn+2OH——2e—=ZnO+H2O |
| C.理论上该电池工作一段时间后,溶液中KOH的浓度不变 |
| D.该电池工作时,电解质中的阴离子向负极移动 |
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源:不详 题型:单选题
 Fe(OH)2+2Ni(OH)2下列推断中正确的是( )
Fe(OH)2+2Ni(OH)2下列推断中正确的是( )| A.①②③ | B.①②④ | C.①③④ | D.②③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

 溶液,则电极反应式为:
溶液,则电极反应式为: 改为稀硫酸做导电物质,则电极反应式为:
改为稀硫酸做导电物质,则电极反应式为: 改为
改为 ,
, 溶液作导电物质,则电极反应式为:
溶液作导电物质,则电极反应式为:查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.13 | B.12 | C.8 | D.1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.反应②在任何温度下均能自发进行 |
| B.CO(g)+2H2(g)=CH3OH(g)△H>-90.5kJ/mol |
| C.甲醇的燃烧热为764kJ/mol |
| D.若CO的燃烧热为282.5kJ/mol,则H2的燃烧热为286kJ/mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
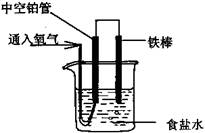
| A.0.1mol Fe完全反应,转移电子0.3mol |
| B.铁作阴极 |
| C.正极反应式为:O2+2H2O+4e-=4OH- |
| D.溶液中的Cl-移向正极 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com