
| A、氧原子数比为1:2 |
| B、体积比为2:1 |
| C、分子个数比为1:2 |
| D、所含原子个数比为1:1 |
| m |
| M |
| 1g |
| 32g/mol |
| 1 |
| 32 |
| 1g |
| 64g/mol |
| 1 |
| 64 |
| 1 |
| 32 |
| 1 |
| 64 |
| 1 |
| 32 |
| 1 |
| 64 |
| 1 |
| 32 |
| 1 |
| 64 |
| 1 |
| 32 |
| 1 |
| 64 |


科目:高中化学 来源: 题型:
| A、溶液中四种离子之间可能满足:c(Cl-)>c(H+)>c(NH4+)>c(OH-) |
| B、若溶液中的溶质是NH4Cl 和NH3?H2O,则离子间可能满足:c(NH4+ )>c(Cl-)>c(OH-)>c(H+ ) |
| C、若溶液中四种离子满足:c(Cl-)>c(NH4+ )>c(H+ )>c(OH-),则溶液中的溶质一定只有NH4Cl |
| D、若溶液中c(Cl-)=c(NH4+),则该溶液一定呈中性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
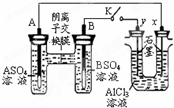 某同学按图所示的装置进行试验.A、B 为两种常见金属,它们的硫酸盐可溶于水.当 K 闭合时,在交换膜处 SO42-从右向左移动.下列分析错误的是( )
某同学按图所示的装置进行试验.A、B 为两种常见金属,它们的硫酸盐可溶于水.当 K 闭合时,在交换膜处 SO42-从右向左移动.下列分析错误的是( )| A、金属活动性A强于B |
| B、B电极反应B-2e-=B2+ |
| C、x电极上有H2产生,发生还原反应 |
| D、反应初期x 电极周围出现白色沉淀,继续实验沉淀将溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、含有离子键的物质一定是离子化合物 |
| B、同素异形体之间的转化是物理变化 |
| C、含有共价键的物质一定是共价化合物 |
| D、气态物质,其微粒间一定存在共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图表示A~E五种物质间的相互转化关系,其中A为淡黄色固体,B为单质.回答下列问题:
如图表示A~E五种物质间的相互转化关系,其中A为淡黄色固体,B为单质.回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com