
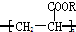 ,下列有关它的说法中,不正确的是( )
,下列有关它的说法中,不正确的是( )| A. | 它可由CH2=CH-COOR经加成聚合反应得到 | |
| B. | 在一定条件下能发生加成反应 | |
| C. | 聚丙烯酸酯材料是一种混合物 | |
| D. | 聚丙烯酸酯是高分子化合物 |
分析 该物质中只含酯基,具有酯的性质,
A.将两个半键连接即得其单体;
B.该物质中不含不饱和键或苯环,不能发生加成反应;
C.n值不同其分子式不同;
D.相对分子质量在10000以上的化合物为高分子化合物.
解答 解:该物质中只含酯基,具有酯的性质,
A.将两个半键连接即得其单体,其单体为CH2=CH-COOR,所以它可由CH2=CH-COOR经加成聚合反应得到,故A正确;
B.该物质中不含不饱和键或苯环,不能发生加成反应,故B错误;
C.n值不同其分子式不同,所以该物质是混合物,故C正确;
D.相对分子质量在10000以上的化合物为高分子化合物,n很大,所以属于高分子化合物,故D正确;
故选B.
点评 本题考查有机物结构和性质,侧重考查学生分析判断能力,明确物质中存在的官能团是解本题关键,易错选项是C.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 还原→取代→加成→消去 | B. | 氧化→加成→取代→消去 | ||
| C. | 消去→加聚→取代→还原 | D. | 还原→消去→加成→取代 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 最外层有2个电子的元素都是金属元素 | |
| B. | 不管哪一个电子层作为最外层,其电子数都不能超过8个 | |
| C. | 在原子核外的电子层中,电子层大的能量低,电子层小的能量高 | |
| D. | 凡单原子形成的离子,一定具有稀有气体元素原子的核外电子排布 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解水生成氢气和氧气时,电能主要转化为化学能 | |
| B. | 风力发电时,风能主要转化为电能 | |
| C. | 煤燃烧时,化学能主要转化为热能 | |
| D. | 白炽灯工作时,电能全部转化为光能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化钠和铁的熔化 | B. | 二氧化硅和生石灰的熔化 | ||
| C. | 碘和干冰的升华 | D. | 食盐和冰的熔化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a>b>c | B. | a>c>b | C. | c>a>b | D. | c>b>a |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
; ,分子内含有极性键.
,分子内含有极性键.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
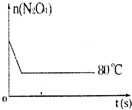 在80℃时,0.40mol的N2O4气体充入2L已经抽空的固定容积的密闭容器中发生如下反应:N2O4?2NO2 △H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
在80℃时,0.40mol的N2O4气体充入2L已经抽空的固定容积的密闭容器中发生如下反应:N2O4?2NO2 △H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:| 时间(s)n(mol) | 0 | 20 | 40 | 60 | 80 | 100 |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com