
钓鱼岛群岛的东海海域及部分太平洋海域探明为海底热水矿床。海底热水矿床是沉积着由岩浆热气从地底喷出的金、铜、锌、稀有金属等区域。下列说法正确的是( )。
A.金不溶于任何溶液
B.铜、锌在空气中均能被氧化成对应的氧化物
C.铜锌合金的熔点低于铜或锌的熔点
D.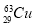 的质子数和中子数之差为34
的质子数和中子数之差为34
科目:高中化学 来源:2014高考名师推荐化学--线索综合4 题型:简答题
工业上以黄铜矿(主要成分CuFeS2)为原料制备金属铜,有如下两种工艺。
I.火法熔炼工艺,将处理过的黄铜矿加人石英,再通人空气进行焙烧,即可制得粗铜。
(1)焙烧的总反应式可表示为2CuFeS2+ 2SiO2+5O2=2Cu+2FeSiO3+4SO2该反应的氧化剂是 。
(2)下列处理SO2的方法,不合理的是_____
A高空排放 B用纯碱溶液吸收制备亚硫酸钠
C用氨水吸收后,再经氧化制备硫酸铵 D用BaCl2溶液吸收制备BaSO3
(3)炉渣主要成分有FeO、Fe2O3、SiO2、Al2O3等,为得到Fe2O3加盐酸溶解后,后续处理过程中,未涉及到的操作有 。
A过滤 B加过量NaOH溶液 C蒸发结晶 D灼烧 E加氧化剂
II. FeCl3溶液浸取工艺其生产流程如下图所示
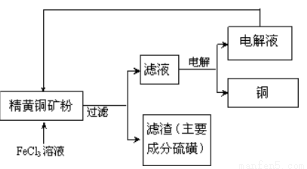
(4)浸出过程中,CuFeS2与FeCl3溶液反应的离子方程式为_____________。
(5)该工艺流程中,可以循环利用的物质是 (填化学式)。
(6)若用石墨电极电解滤液,写出阳极的电极反式_____________。
(7)黄铜矿中含少量Pb,调节C1一浓度可控制滤液中Pb2+的浓度,当c(C1一)=2mo1·L-1时,溶液中Pb2+物质的量浓度为 mol·L-1。[已知KSP(PbCl2)=1 x 10一5]
查看答案和解析>>
科目:高中化学 来源:2014江苏常熟市高二化学期末模拟4(必修2、选修4、结构)试卷(解析版) 题型:填空题
(16分)工业上可用煤制天然气,生产过程中有多种途径生成CH4。
(1)写出CO2与H2反应生成CH4和H2O的热化学方程式 。
已知: ① CO(g)+H2O(g) H2(g)+CO2(g) ΔH=-41kJ·mol-1
H2(g)+CO2(g) ΔH=-41kJ·mol-1
② C(s)+2H2(g) CH4(g) ΔH=-73kJ·mol-1
CH4(g) ΔH=-73kJ·mol-1
③ 2CO(g) C(s)+CO2(g) ΔH=-171kJ·mol-1
C(s)+CO2(g) ΔH=-171kJ·mol-1
(2)另一生成CH4的途径是CO(g)+3H2(g) CH4(g)+H2O(g)。其他条件相同时,H2的平衡转化率在不同压强下随温度的变化如图所示。
CH4(g)+H2O(g)。其他条件相同时,H2的平衡转化率在不同压强下随温度的变化如图所示。
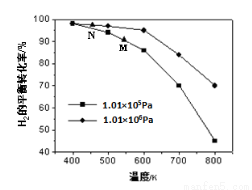
①该反应的△H 0(填“<”、“=”或“>”)。
②实际生产中采用图中M点而不是N点对应的反应条件,运用化学反应速率和平衡知识,同时考虑生产实际,说明选择该反应条件的理由________________________。
③某温度下,将0.1 mol CO和0.3 mol H2充入10L的密闭容器内发生反应CO(g)+3H2(g)  CH4(g)+H2O(g),平衡时H2的转化率为80%,求此温度下该反应的平衡常数K。(写出计算过程,计算结果保留两位有效数字)
CH4(g)+H2O(g),平衡时H2的转化率为80%,求此温度下该反应的平衡常数K。(写出计算过程,计算结果保留两位有效数字)
查看答案和解析>>
科目:高中化学 来源:2014年高考化学鲁科版复习专练1气体定量测定在实验中应用练习卷(解析版) 题型:实验题
饱和氯水与石灰石反应是制取较浓HClO溶液的方法之一。某兴趣小组进行了如下实验探究。
实验一:定性研究。
①在试管中加入过量的块状碳酸钙,再加入约20 mL饱和氯水(如图所示),充分反应,有少量气泡产生,溶液浅黄绿色退去;
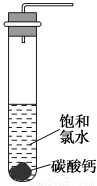
②过滤,将滤液滴在有色布条上,发现滤液比氯水的漂白性更强;
③为了确定反应产物,将滤液分为三份,分别进行以下实验:
第一份与石灰水混合,立即产生大量白色沉淀;
第二份与稀盐酸混合,立即产生大量无色气体;
第三份滤液加热,看到滤液变浑浊且有大量无色气体产生。经检测,上述实验中产生的无色气体均为CO2。
请回答:
(1)反应后所得的溶液漂白性比氯水强的原因是 。
(2)依据上述实验可推知:滤液中的溶质除CaCl2、HClO外,还有 (填写溶质的化学式)。
实验二:定量研究。
在圆底烧瓶底部,用一塑料网包住块状石灰石(过量)与150 mL饱和氯水反应,按下图所示装置实验,待不再产生气泡后,将塑料网中剩余的石灰石提出液面,将装置密封后再加热,煮沸烧瓶中的液体,量筒中的气体不再增加时停止实验。
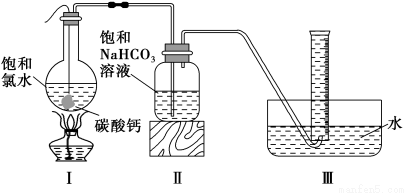
请回答:
(3)实验结束后检测到量筒中收集到的气体除CO2外还有O2,请写出Ⅰ中产生O2的化学反应方程式 。
(4)为减少用装置Ⅲ收集气体过程中CO2因溶解而造成的损失,请你对装置Ⅲ进行改进(水槽中仍为水),最简单的方法是 。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学鲁科版4.3铜及其化合物 金属材料与复合材料练习卷(解析版) 题型:填空题
历史上金、银、铜主要是作为货币金属或装饰品被应用。
(1)金、银、铜常被作为钱币流通,从化学角度来看,主要是利用它们的 。
A.硬度适中
B.密度适中
C.在自然界里都可得到纯净的单质
D.不活泼性
(2)一位收藏者有一枚表面是黑色,且有少量绿色锈状物的货币,这肯定是 币,黑色物质是 ,形成这种物质的化学方程式为 ,绿色物质是 ,形成这种物质的化学方程式为 ,这枚金属币的真面目为 色。另外一枚是闪闪发光的黄色金属币,它肯定是 币,表面一直未被氧化的原因是 。
(3)不法分子有时用铜锌合金制成假金币行骗。下列方法中能有效鉴别其真假的是 。
A.观察颜色
B.查看图案
C.用手掂量轻重
D.滴一滴硝酸在币的表面,观察现象
查看答案和解析>>
科目:高中化学 来源:2014年高考化学鲁科版4.1硅 无机非金属材料练习卷(解析版) 题型:填空题
已知A、B、C、D、E、F、G、H可以发生如下图所示的转化,反应中部分生成物已略去。其中,A、G为同一主族元素的单质,B、C、H在通常情况下为气体,化合物C是一种形成酸雨的大气污染物。
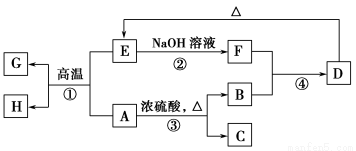
请填空:
(1)写出E的两种用途 、 。
(2)反应②的离子方程式为 。
(3)反应③的化学方程式是 。
(4)反应④的离子方程式是 。
(5)写出一个由A生成H的置换反应方程式: 。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学鲁科版4.1硅 无机非金属材料练习卷(解析版) 题型:选择题
在①浓硝酸;②水;③浓硫酸;④氢氟酸;⑤氢氧化钾溶液中,能与单质硅起化学反应的是( )。
A.①② B.②④ C.④⑤ D.③④
查看答案和解析>>
科目:高中化学 来源:2014年高考化学鲁科版3.3硫的转化练习卷(解析版) 题型:填空题
近年来,酸雨污染较为严重,防治酸雨成了迫在眉睫的问题。
(1)有人提出了一种利用氯碱工业产品处理含二氧化硫废气的方法,流程如下:
(Ⅰ)将含SO2的废气通入电解饱和食盐水后所得到的溶液中,得NaHSO3溶液。
(Ⅱ)将电解饱和食盐水所得气体反应后制得盐酸。
(Ⅲ)将盐酸加入NaHSO3溶液中,反应所得到的SO2气体回收,生成的NaCl循环利用。
①写出步骤(Ⅰ)反应的化学方程式: 。
②写出步骤(Ⅱ)中电解饱和食盐水的化学方程式: 。
③写出步骤(Ⅲ)反应的离子方程式: 。
(2)还有学者提出利用Fe2+、Fe3+等离子的催化作用,常温下将SO2氧化成SO42-而实现SO2的回收利用。某研究性学习小组据此设计了如下方案,在实验室条件下测定转化器中SO2氧化成SO42-的转化率。

①该小组采用下图装置在实验室测定模拟烟气中SO2的体积分数,X溶液可以是 。(填写序号)
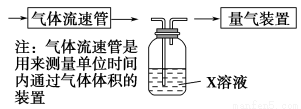
A.碘的淀粉溶液B.酸性高锰酸钾溶液
C.氢氧化钠溶液D.氯化钡溶液
②若上述实验是在标准状况下进行的,欲测定转化器中SO2氧化成SO 的转化率,已知气体流速,还需测定的数据有 、 。
的转化率,已知气体流速,还需测定的数据有 、 。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学鲁科版2.5铁及其化合物练习卷(解析版) 题型:选择题
下列关于铁的叙述正确的是( )。
①铁能被磁铁吸引,但纯铁易被腐蚀
②在人体内的血红蛋白中含有铁元素
③铁位于元素周期表中第四周期第ⅧB族
④铁能在氧气中剧烈燃烧,但不能在水蒸气中燃烧
⑤铁与强氧化剂硝酸反应的产物仅是Fe(NO3)3
⑥不能通过化合反应制得FeCl2和Fe(OH)3
A.①③ B.②④ C.②⑤ D.④⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com