
 ФД¶БїміµПµБРґр°ё
ФД¶БїміµПµБРґр°ё
| Дкј¶ | ёЯЦРїОіМ | Дкј¶ | іхЦРїОіМ |
| ёЯТ» | ёЯТ»Гв·СїОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СїОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СїОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СїОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СїОіМНЖјцЈЎ | іхИэ | іхИэГв·СїОіМНЖјцЈЎ |
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
A.ИЬЅвЙЩБїКіСОУЪЛ®ЦРЈ¬¦¤SЈѕ0?
B.МјєНСхЖш·ґУ¦ЙъіЙCO(g)Ј¬¦¤SЈѕ0?
C.H2O(g)±діЙТєМ¬Л®Ј¬¦¤SЈѕ0?
D.CaCO3(s)јУИИ·ЦЅвОЄCaOЈЁsЈ©єНCO2ЈЁgЈ©Ј¬¦¤SЈѕ0?
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє2015ЅмЦШЗмКРёЯ¶юЙПС§ЖЪЖЪЦРїјКФ»ЇС§КФѕнЈЁЅвОц°жЈ© МвРНЈєМоїХМв
ДСИЬРФФУВ±КЇ(K2SO4Ў¤MgSO4Ў¤2CaSO4Ў¤2H2O)КфУЪЎ°ґфїуЎ±Ј¬ФЪЛ®ЦРґжФЪИзПВИЬЅвЖЅєвЈє
K2SO4Ў¤MgSO4Ў¤2CaSO4Ў¤2H2O(s) 2Ca2Ј«Ј«2KЈ«Ј«Mg2Ј«Ј«4SO42-Ј«2H2OЎЈОЄДЬід·ЦАыУГјШЧКФґЈ¬УГ±ҐєНCa(OH)2ИЬТєИЬЅюФУВ±КЇЦЖ±ёБтЛбјШЈ¬№¤ТХБчіМИзПВЈє
2Ca2Ј«Ј«2KЈ«Ј«Mg2Ј«Ј«4SO42-Ј«2H2OЎЈОЄДЬід·ЦАыУГјШЧКФґЈ¬УГ±ҐєНCa(OH)2ИЬТєИЬЅюФУВ±КЇЦЖ±ёБтЛбјШЈ¬№¤ТХБчіМИзПВЈє
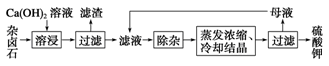
ЈЁ1Ј©ВЛФьЦчТЄіЙ·ЦУР________єНCaSO4ТФј°ОґИЬФУВ±КЇЎЈ
ЈЁ2Ј©УГ»ЇС§ЖЅєвТЖ¶ЇФАнЅвКНCa(OH)2ИЬТєДЬИЬЅвФУВ±КЇЅюіцKЈ«µДФТтЈє
ЎЈ
ЈЁ3Ј©Ў°іэФУЎ±»·ЅЪЦРЈ¬ПИјУИл ИЬТєЈ¬ѕЅБ°иµИІЩЧчєуЈ¬№эВЛЈ¬ФЩјУИл ИЬТєµчВЛТєpHЦБЦРРФЎЈ
ЈЁ4Ј©І»Н¬ОВ¶ИПВЈ¬KЈ«µДЅюіцЕЁ¶ИУлИЬЅюК±јдµД№ШПµјыУТНјЎЈУЙНјїЙµГЈ¬ЛжЧЕОВ¶ИЙэёЯЈ¬
ўЩ Ј¬
ўЪ Ј¬

ўЫИЬЅюіцµДKЈ«µДЖЅєвЕЁ¶ИФцґуЎЈ
ЈЁ5Ј©УРИЛТФїЙИЬРФМјЛбСООЄИЬЅюјБЈ¬ФтИЬЅю№эіМЦР»б·ўЙъЈєCaSO4(s)Ј«CO32- CaCO3(s)Ј«SO42-ЎЈТСЦЄ298 KК±Ј¬Ksp(CaCO3)ЈЅ2.80ЎБ10Ј9Ј¬Ksp(CaSO4)ЈЅ4.90ЎБ10Ј5Ј¬јЖЛгґЛОВ¶ИПВёГ·ґУ¦µДЖЅєвіЈКэЈ¬KЈЅ
ЎЈ
CaCO3(s)Ј«SO42-ЎЈТСЦЄ298 KК±Ј¬Ksp(CaCO3)ЈЅ2.80ЎБ10Ј9Ј¬Ksp(CaSO4)ЈЅ4.90ЎБ10Ј5Ј¬јЖЛгґЛОВ¶ИПВёГ·ґУ¦µДЖЅєвіЈКэЈ¬KЈЅ
ЎЈ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє2014ЅмХгЅКЎёЯ¶юПВС§ЖЪЖЪЦРїјКФ»ЇС§КФѕнЈЁЅвОц°жЈ© МвРНЈєСЎФсМв
ПВБР±д»Ї№эіМЦРЈ¬¦¤SЈј0µДКЗ
AЈ®ВИ»ЇДЖИЬУЪЛ®ЦРЎЎ BЈ®NH3(g)єНHCl(g)·ґУ¦ЙъіЙNH4Cl
CЈ®ёЙ±щµДЙэ»ЄЎЎ DЈ®CaCO3(S)·ЦЅвОЄCaO(S)єНCO2(g)
Ійїґґр°ёєНЅвОц>>
№ъјКѧУУЕСЎ - Б·П°ІбБР±н - КФМвБР±н
єю±±КЎ»ҐБЄНшОҐ·ЁєНІ»БјРЕПўѕЩ±ЁЖЅМЁ | НшЙПУРє¦РЕПўѕЩ±ЁЧЁЗш | µзРЕХ©ЖѕЩ±ЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРє¦РЕПўѕЩ±ЁЧЁЗш | ЙжЖуЗЦИЁѕЩ±ЁЧЁЗш
ОҐ·ЁєНІ»БјРЕПўѕЩ±Ёµз»°Јє027-86699610 ѕЩ±ЁУКПдЈє58377363@163.com