
分析 (1)处于同周期的相邻两种元素A和B,A的最高价氧化物的水化物的碱性比B弱,说明金属性A<B,同周期随原子序数增大金属性减弱、原子半径减小;
(2)处于同主族的相邻两种非金属元素,元素的原子核外电子层数越少,原子半径越小,元素的非金属性就越强,其最高价氧化物对应的水化物的酸性就越强.若B的原子序数为x且核外电子层数为3,则A位于第四周期,处于过渡元素之后,原子序数相差第四周期容纳的元素种数18种.
解答 解:(1)处于同周期的相邻两种元素A和B,A的最高价氧化物的水化物的碱性比B弱,说明金属性A<B,同周期随原子序数增大金属性减弱、原子半径减小,则原子序数A>B,故A处于B的右边,B的原子半径比A大,若B的最外层有x个电子,则A最外层有(x+1)个电子,
故答案为:右;大;(x+1);
(2)处于同主族的相邻两种非金属元素,元素的原子核外电子层数越少,元素的非金属性就越强,其最高价氧化物对应的水化物的酸性就越强.由于A的最高价氧化物的水化物的酸性比B弱,A处于B的下边,元素的原子核外电子层数越多,原子半径就越大,所以B的原子半径比A小.若B的原子序数为x且核外电子层数为3,则A位于第四周期,处于过渡元素之后,第四周期包括的元素种数是18种,则A的原子序数为x+18,
故答案为:下;小;x+18.
点评 本题考查元素周期表与元素周期律,熟练掌握元素周期律应用,注意理解同主族原子序数关系,掌握元素周期表中列与族的关系.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  用石斧解剖 | B. |  早期的农业耕作 | C. |  简单机械织布 | D. |  祥云火炬燃烧 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同温下分别在100g水中最多能溶解的无水CuSO4和CuSO5•5H2O的质量 | |
| B. | 纯水在25℃和90℃时的pH值 | |
| C. | 25℃时,等体积的pH都等于3的盐酸和AlCl3溶液中,已电离的水分子数 | |
| D. | 在反应NH3+NO→N2+H2O中,被氧化和被还原的N原子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH${\;}_{4}^{+}$、SO${\;}_{4}^{2-}$、CO${\;}_{3}^{2-}$、K+ | B. | K+、Cl-、Na+、SO${\;}_{4}^{2-}$ | ||
| C. | Mg2+、NO${\;}_{3}^{-}$、K+、Cl- | D. | Na+、Ba2+、Ca2+、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
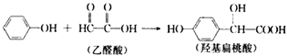
| A. | 该反应是加成反应 | |
| B. | 1 mol羟基扁桃酸能与3mol NaOH反应 | |
| C. | 乙醛酸与H2加成的产物能在催化剂作用下形成高分子化合物 | |
| D. | 苯酚和羟基扁桃酸遇上FeCl3溶液都会显色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | M的单质能够用来制造光导纤维 | |
| B. | Z、W、M的氧化物均可做耐高温材料 | |
| C. | 工业上常用电解熔融氯化物的方法制备Z、W的单质 | |
| D. | Y的单质都有剧毒,而且其着火点低,常保存在冷水中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
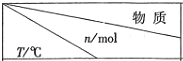 | 活性炭 | NO | E | F |
| T1 | 2.000 | 0.040 | 0.030 | 0.030 |
| T2 | 2.005 | 0.050 | 0.025 | 0.025 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com