
��������ˮ��Һ�׳�˫��ˮ���е��ˮ�ߣ����⡢�ȼ��ؽ���������Ⱦ�������ֽ⡣
��1��ij�Լ������Ƶ�7%~8%��˫��ˮ��������Ũ����30%����Һ�����˷�����
����д��ţ���
a����ѹ���� �� b����ѹ���� c��������ʯ�ҳ�ѹ���� ���� d����ѹ����
��2������õ���˫��ˮ����Ԫ�صĺ���Ϊ90%�����������Ĵ���Ϊ ��������֪�������ڿ�����ȼ������ˮ����������������ڿ�����ȼ��Ҳ��������H2O2����������¶��ֽ��ˡ�Ϊ����֤�����ڿ�����ȼ�յIJ������Ƿ���H2O2��ij����С��ͬѧ��Ƶ�ʵ��װ�ü�ͼ-1��
��3����ͬѧ�����ͼ-2�Ģ٣�����ѡȡ���ͼ��1�����е�װ�ã����е��� ����д��ţ���
��4������ͬѧ�����Ը��������Һ����H2O2�Ĵ��ڣ���ɸ÷�Ӧ�����ӷ���ʽ��
�� + �� Mn2+ + H2O
��ͬѧ���ҵļ��鷽����������ɣ���п����ϡ����ķ�Ӧ�в���������H2S�Ȼ�ԭ�����壬Ҳ��ʹ���Ը��������Һ��ɫ�������ͬѧ��ʵ�鷽������Ľ����飺 ��
��5����̼���ƣ�2Na2CO3?3H2O2���׳ƹ���˫��ˮ�����ֽ⣬��ֽⷴӦ�Ļ�ѧ����ʽ�ɱ�ʾΪ��2 (2Na2CO3?3H2O2) �� 4Na2CO3 + 6H2O + 3O2��
ȡһ�����Ĺ�̼�������ܱ�������ʹ����ȫ�ֽ⣬�����������12.0g����ȴ�����º������ò����м�ˮ���Ƴ�10.6% ��Na2CO3��Һ�����ˮ g��
��1��b��2�֣�
��2��21.25%����2�֣�д0.2125��ȫ�֣�
��3���ڣ�2�֣�
��4��2MnO4-+5H2O2+6H+��2Mn2++5O2��+8H2O��2�֣�������ȷдȫ1�֣���ƽ1�֣���
�Ƚ��Ƶõ�����ͨ��װ�м�ʯ�ҵĸ���ܣ�Ȼ���ȼ�������������֣���2�֣�
��5��433.5g��2�֣�
���������������1��˫��ˮ���Ȼ�ֽ⣬ֻ��ͨ����ѹ�����¶Ⱥ������Է���ֽ⣻
��2��˫��ˮ�к����������У�H2O2��H2O�������ʵ����ֱ�Ϊx��y������˫��ˮ����Ԫ�صĺ���Ϊ90%�����������Ĵ���Ϊ��ʾΪ��16/90%="18y+34x" ,(2x+3y)*16/(34x+18y)=90%,����ã�2x+y=1,��x=9-8/0.9�����34x/(34x+18y)=21.25%��
��3��ͼ��1�����е�װ������������װ�ã������������Ǣڣ�����ͨ��ʹ��Һ����Ӷ�ʹ��Ӧֹͣ������
��4������������ԭ��Ӧԭ������д��2MnO4-+5H2O2+6H+��2Mn2++5O2��+8H2O���൱����֤�������Ƿ���H2S���壬���ѻ������ͨ�뵽����ͭ��Һ����������ɫ����������H2S���塣Ҳ�����Ƚ��Ƶõ�����ͨ��װ�м�ʯ�ҵĸ���ܣ�Ȼ���ȼ��
��5�����ݷ���ʽ2 (2Na2CO3?3H2O2) �� 4Na2CO3 + 6H2O + 3O2������������������12.0gʱ������̼����12*4*106/(3*32)=53g������ˮ������Ϊ��(0.5*6/4)*18=13.5g��Ҫ���Ƴ�10.6% ��Na2CO3��Һ�����ˮ(53/0.106 )-53-13.5=433.5g��
���㣺���⿼����ʵ��ԭ���ķ�����������ԭ��Ӧ����ʽ����ƽ����Һ���������ļ��㡣



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�⻯��ͭ(CuH)��һ����������,��CuSO4��Һ�͡���һ���ʡ���40��50 ��ʱ��Ӧ����������CuH���ȶ�,�ֽ�;����������ȼ��;��ϡ���ᷴӦ����������;Cu+�����������·����ķ�Ӧ��2Cu+ Cu2++Cu������������Ϣ,����Լ������յĻ�ѧ֪ʶ,�ش�:
Cu2++Cu������������Ϣ,����Լ������յĻ�ѧ֪ʶ,�ش�:
(1)��CuSO4��Һ�͡���һ���ʡ���CuH�ķ�Ӧ��,��������ԭ�۵����,�⡰��һ���ʡ��ڷ�Ӧ�������������������������������������
(2)д��CuH��������ȼ�յĻ�ѧ��Ӧ����ʽ
(3)CuH�ܽ���ϡ���������ɵ���������������,�����Ӧ�������˱�״����22.4 L������,����ԭ�����ӵõ��ӵ����ʵ���������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�ۻƣ�As4S4���ʹƻƣ�As2S3������ȡ�����Ҫ����ԭ�ϣ���������Ȼ���й����������������������գ�
��1��As2S3��SnCl2�������з�Ӧת��ΪAs4S4��SnCl4���ų�H2S���塣��As2S3��SnCl2������ȫ��Ӧ��As2S3��SnCl2�����ʵ���֮��Ϊ______��
��2��������Ӧ�е���������______����Ӧ�������������______���ա�
��3��As2S3��HNO3�����·�Ӧ��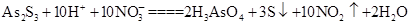 ��������2 mol H3AsO4����Ӧ��ת�Ƶ��ӵ����ʵ���Ϊ______�������÷�Ӧ��Ƴ�һԭ��أ���NO2Ӧ����______����������������������ݳ���
��������2 mol H3AsO4����Ӧ��ת�Ƶ��ӵ����ʵ���Ϊ______�������÷�Ӧ��Ƴ�һԭ��أ���NO2Ӧ����______����������������������ݳ���
��4������Ӧ����NO2��11.2 L O2����״������Ϻ���ˮ����ȫ��ת����Ũ���ᣬȻ���������C��Ӧ����������CO2����______��ѡ���ţ���
a����0.5 mol
b������0.5 mol
c������0.5 mol
d����ȷ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
ʵ�����ﳣ��Ũ������������̷�Ӧ����ȡ��������������Ӧ�Ļ�ѧ����ʽΪ��
MnO2��4HCl(Ũ)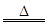 MnCl2��Cl2����2H2O
MnCl2��Cl2����2H2O
��1����Ӧ���У���������________�����ϼ����ߵ�Ԫ����________��
��2��ȡһ�������Ũ������MnO2������Ӧ�������������ڱ�״���µ����Ϊ1.12 L(����Cl2���ܽ�)����μӷ�Ӧ��HCl�����ʵ�����________����Ӧ�б�������HCl��������________��(д����Ҫ�������)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��Ԫ��ʮ����Ҫ���䵥�ʼ��仯�����ڿ��С�������������ʮ�ֹ㷺����;��
��1����Ԫ�غ�������Ų�ʽΪ�� ��ԭ�Ӻ���� �ֲ�ͬ�ܼ��ĵ��ӣ���ԭ�Ӻ���������� �ֲ�ͬ����չ������ �ֲ�ͬ�˶�״̬�ĵ��ӡ�
��2�����¡��˹��̵������о����������³�ѹ�����������£�N2�ڴ���������ˮ������Ӧ��
2N2 (g)+6H2O (l) 4NH3 (g)+3O2 (g) - Q �������Ӧ��ƽ�ⳣ��Kֵ��÷�Ӧ ��ѡ���ţ���
4NH3 (g)+3O2 (g) - Q �������Ӧ��ƽ�ⳣ��Kֵ��÷�Ӧ ��ѡ���ţ���
A��һ��������Ӧ�����ƶ�
B����ƽ���ƶ�ʱ����Ӧ������������С
C��һ�����淴Ӧ�����ƶ�
D����ƽ���ƶ�ʱ�淴Ӧ�����ȼ�С������
��3�����������Ӧ�����������ܱ������н��У�����Ӧ�ﵽƽ��������жϴ������
A�������������ƽ������������ʱ����仯 B��ͨ�����ϡ����������߷�Ӧ������
C��������������ܶȲ���ʱ����仯 D��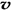 ��N2��/
��N2��/ 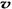 ��O2��=2:3
��O2��=2:3
��4�����������Ϊ���ȼ�ϵ���Ҫ�����塣��������ڸ�ѹ��450���������Ѹ�ٷֽ⣬��Ӧ�Ļ�ѧ����ʽ4NH4ClO4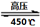 6H2O��+ 2N2��+ 4HCl��+ 5O2�����������������뻹ԭ��������ʵ���֮���� ��ÿ�ֽ�1mol������泥�ת�Ƶĵ�����Ŀ�� ��
6H2O��+ 2N2��+ 4HCl��+ 5O2�����������������뻹ԭ��������ʵ���֮���� ��ÿ�ֽ�1mol������泥�ת�Ƶĵ�����Ŀ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
���Ṥ���������к���SO2���ж��ַ�����ʵ����������
��1����ҵ������Ĺ����У�SO2�����������Ļ�ѧ����ʽΪ ��
��2����ʪʽ���շ����������ռ���SO2������Ӧ�Ӷ�����
��֪��25��ʱ��H2SO3  HSO3 -+H+ K=1.5��10-2
HSO3 -+H+ K=1.5��10-2
H2CO3 HCO3 -+H+ K=4.4��10-7
HCO3 -+H+ K=4.4��10-7
�����Լ����ʺ������÷����ռ����� ������ĸ��ţ���
a.ʯ���� b. Na2SO3��Һ c. Na2CO3��Һ
�ڡ��Ƽ����NaOH��Һ�����ռ�����100 mL 0.2 mol��L-1��NaOH��Һ��ͨ���״����0.448 L SO2���壬��Ӧ������ҺpH<7������Һ�����и�����Ũ�ȹ�ϵ��ȷ���� ������ĸ��ţ���
a.c(HSO3-)> c(SO32-)> c(H2SO3)
b.c(Na+)>c(HSO3-)> c(H+)> c(SO32-)
c.c(Na+)+c(H+)= c(HSO3-)+c(SO32-)+c(OH-)
��3��ij���᳧��������������Cr2O72-�����Է�ˮ���������ͬʱ�Ʊ�Cr2O3��Ʒ�������������£�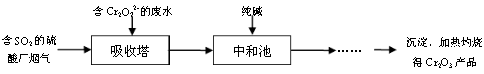
���������з�Ӧ��ĸ�Ԫ����Cr3+��ʽ���ڣ������з�����Ӧ�����ӷ���ʽΪ ��
���кͳ��еķ�Ӧ������Cr(OH)3�����⣬�������ij�����壬������Ļ�ѧʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
ij��ѧ��Ӧ�ķ�Ӧ��Ͳ������£�Al��NaNO3��H2O Al(OH)3��N2��NaAlO2
Al(OH)3��N2��NaAlO2
��1���÷�Ӧ����������______________��
��2���÷�Ӧ������������_______________��
��3����Ӧ������ת��5 mol e�������ɱ�״����N2�����________L��
��4����ƽ�÷�Ӧ�Ļ�ѧ����ʽ��
______Al��_____NaNO3��_____H2O==______Al(OH)3��______N2��______NaAlO2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��֪��Ӧ��3Cl2+8NH3==N2+6NH4Cl
��1������71gCl2�μӷ�Ӧ���������������� ��ת�Ƶ��ӵ����ʵ���Ϊ mol��
��2����Ӧ��������14g N2������ g NH3��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
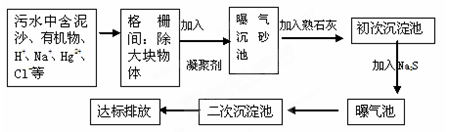
ˮ����������ͷ�չ�ı�����Դ����ˮ�ʵ���Ⱦ����ȴԽ��Խ���ء�Ŀǰ����������Ѹ߶�����������⣬����ȡ������ʩ����������
��1����ҵ��ˮ�г����в�ͬ���͵���Ⱦ��ɲ��ò�ͬ�ķ������������´�����ʩ�ͷ�������ȷ����________������ĸ��ţ��ɶ�ѡ����
| ѡ�� | ��Ⱦ�� | ������ʩ | ������� |
| A | ���� | ����ʯ���к� | ������ |
| B | Cu2+���ؽ������� | �������γ��� | ��ѧ�� |
| C | ������ķ�ˮ | ��ʯ��ˮ��Ӧ | ��ѧ�� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com