
下列说法正确的是
A.金属在反应中只能作还原剂,非金属在反应中只能作氧化剂
B.氧化剂在反应中失去电子,还原剂在反应中得到电子
C.氧化剂具有氧化性,还原剂具有还原性
D.阳离子只有氧化性,阴离子只有还原性
科目:高中化学 来源:2016届黑龙江省高三上学期第一次月考化学试卷(解析版) 题型:选择题
实验室中以下物质的贮存方法,不正确的是
A.保存硫酸亚铁溶液时,向其中加入铁钉和少量硫酸
B.少量金属锂保存在煤油中
C.少量液溴可用水封存,防止溴挥发
D.浓硝酸用带玻璃塞的细口、棕色试剂瓶盛放,并贮存在阴凉处
查看答案和解析>>
科目:高中化学 来源:2016届河南省三门峡市高三上学期第一次精英对抗赛化学试卷(解析版) 题型:选择题
下列离子方程式正确的是( )
A、硫酸铝溶液与过量Ba(OH)2溶液反应
2Al3+ + 3SO42- +3 Ba2++8OH-=3BaSO4↓+2A1O2- +4H2O
B、碳酸钠溶液中滴加盐酸至恰好要出现气泡时停止:
CO32-+2H+=CO2↑+H2O
C、酸性高锰酸钾溶液与H2O2溶液混合:
2MnO4-+3H2O2+6H+=2Mn2++6H2O+402↑
D、氯气通入亚硫酸钠溶液中:2Cl2+SO32-+H2O=2Cl-+SO2↑+2HClO
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省邯郸市高一上第一次月考化学试卷(解析版) 题型:选择题
下列叙述中正确的是
①标准状况下,1 L HCl和1 L H2O的物质的量相同;
②标准状况下,11.2 L H2和14 g N2所含原子数相同;
③28 g CO的体积约为22.4 L;
④两种物质的物质的量相同,则它们在标准状况下的体积相同;
⑤同温同体积时,气体物质的物质的量越大,则压强越大;
⑥同温同压下,气体的密度与气体的相对分子质量成正比。
A.仅⑤⑥ B.仅②⑤⑥
C.仅②③⑤⑥ D.仅①②④⑤⑥
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三上学期第一次月考化学试卷(解析版) 题型:简答题
(9分)高铁酸钠是一种高效多功能水处理剂。工业上常采用NaClO氧化法生产,反应原理为:在碱性条件下,利用NaClO氧化Fe(NO3)3制得Na2FeO4,过滤得到粗产品,再用NaOH溶液溶解,重结晶,用有机溶剂脱碱,低温烘干得到固体样品。反应方程式为:
3NaClO + 2Fe(NO3)3 + 10NaOH=2Na2FeO4↓+ 3NaCl + 6NaNO3 + 5H2O
(1)上述制备过程中,用NaOH溶液溶解粗产品而不用水的原因是 。
(2)高铁酸钠电池是一种新型可充电电池,电解质为NaOH溶液,放电时负极材料为Zn,正极产生红褐色沉淀,写出该电池反应方程式 。
(3)生产高铁酸钠的原料之一Fe(NO3)3用黑色粉末Fe(含有Fe3O4)与稀硝酸反应制备。准确称取该黑色粉末13.12g,加入200mL 4 mol·L-1 HNO3搅拌,固体完全溶解,共收集到标准状况下2688mL的气体,经分析其中只含有NO,并测得此时溶液中c(H+)=0.4mol·L-1(设反应前后溶液体积不变)。通过以上数据,计算该黑色粉末中Fe的质量分数。(写出计算过程,结果保留两位小数)
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列有关化学用语的表示正确的是
A.甲烷分子的球棍模型:
B.HClO的结构式:H-Cl-O
C.质子数为53,中子数为78的碘原子: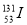
D.熔融状态下硫酸氢钾的电离方程式:KHSO4  K++H++SO42-
K++H++SO42-
查看答案和解析>>
科目:高中化学 来源:2016届河北省冀州市高三复习班上第一次月考化学试卷A(解析版) 题型:实验题
(10分)已知SiO2、SO2和CO2都是酸性氧化物,化学性质具有一定的相似性;
Mg和Na的化学性质也具有一定相似性。
I、用如图所示装置进行Mg与SO2反应的实验。
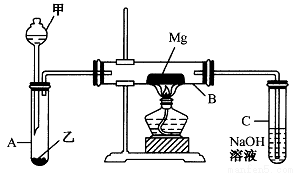
(1)选择制取SO2的合适试剂____________。
①10%的H2SO4溶液 ②70%的H2SO4溶液 ③Na2SO3固体 ④CaSO3固体
(2)写出装置B中发生的主要反应的化学方程式___________。
装置C中NaOH溶液的作用是______________。
(3)该装置仍有不足之处,请说明_______________。
Ⅱ、某研究小组进行了“实验室制Si”的研究,它们以课本为基础,查阅资料得到以下可供参考的四条信息:
①Mg在加热的条件下即可与SiO2反应
②金属硅化物与稀H2SO4反应生成硫酸盐与SiH4
③Si和SiO2均不与稀H2SO4反应
④SiH4在空气中自燃
他们在研究报告中记载着“……选用合适的物质在适宜的条件下充分反应;再用足量稀硫酸溶解固体产物;然后过滤、洗涤、干燥;最后称量……在用稀硫酸溶解固体产物时,发现有爆鸣声和火花,其产率也只有预期值的63%左右”。
(4)该小组“实验室制Si”的化学方程式是 。
(5)你估计“用稀硫酸溶解固体产物时,发现有爆鸣声和火花”的原因是(用化学方程式说明): 。
查看答案和解析>>
科目:高中化学 来源:2016届河北省高三上学期二调化学试卷(解析版) 题型:实验题
(10分)资料表明,硫粉与热的KOH溶液共热生成两种盐,其中一种是K2SO3。某化学兴趣小
组进行该实验时,却检测到生成的盐中含有SO42-。
(1)兴趣小组同学认为,上述反应的生成物可能与反应温度(T),KOH溶液的浓度(c)有关。他们做了如下对比实验(每次实验中硫粉的质量、KOH溶液的体积均相同)。
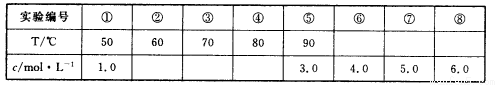
实验①~④是探究温度对生成物的影响,⑤~⑧是探究KOH溶液的浓度对生成物的影响。请在表中相应空格内填人相应数据。
(2)兴趣小组设计实验对上述反应中生成的盐的成分进行探究。他们提出如下假设,请你根据氧化还原反应的规律,完成假设二和假设三:
假设一:生成的盐是K2S和K2 S03;
假设二:生成的盐是____;
假设三:生成的盐是____;
(3)请你设计实验验证上述假设一。完成下表中内容。[除了硫粉与热的KOH溶液的反应液之外,可供选择的药品有稀硝酸,稀盐酸等;已知:6H++SO32-+2S2-=3S+3H2O
(4)兴趣小组通过改变硫粉的质量,得出生成钾盐的质量与硫粉质量的变化关系如图所示。有人据此得出结论:生成的盐一定是K2S和K2SO3的混合物。请你根据计算结果指出该结论是否正确 。
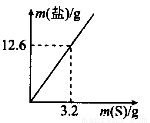
(5)请分析上述反应中有K2S04生成的可能原因是 。
查看答案和解析>>
科目:高中化学 来源:2016届河南省高三第四次大考化学试卷(解析版) 题型:选择题
有一未知的无色溶液,只可能含有以下离子中的若干种(忽略由水电离产生的H+、OH-):H+、NH4+、K+、Mg2+、Cu2+、Al3+、NO3-、CO32-、SO42-,现取三份100mL溶液进行如下实验:
①第一份加足量AgNO3溶液后,有白色沉淀产生。
②第二份加足量BaCl2溶液后,有白色沉淀产生,经洗涤、干燥后,沉淀质量为6.99 g。
③第三份逐滴滴加NaOH溶液,测得沉淀与NaOH溶液的体积关系如图。
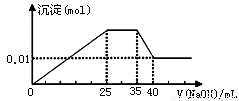
根据上述实验,以下推测不正确的是
A.原溶液一定不存在H+、Cu2+、CO32-
B.不能确定原溶液是否含有K+、NO3-
C.实验所加的NaOH的浓度为2mol·L-1
D.原溶液确定含Mg2+、Al3+、NH4+,且n(Mg2+):n(Al3+):n( NH4+)=1:1:2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com