
分析 (1)根据化合价的变化判断电子的转移方向和数目;
(2)根据方程式,结合硫酸的物质的量计算剩余H+的物质的量浓度.
解答 解:(1)反应中Al的化学键由0价升高为+3价,H元素的化合价由+1价降低到0价,氧化剂为H2SO4,还原剂为Al,
用双线桥法可表示如下: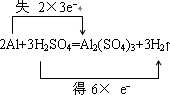
答: ;
;
(2)n(H2SO4)=0.5L×3mol/L=1.5mol,n(H2)=$\frac{11.2L}{22.4L/mol}$=0.5mol,
2Al+3H2SO4=Al2(SO4)3+3H2↑
0.5mol 0.5mol
所以剩余硫酸的物质的量为1.5mol-0.5mol=1mol,
则:反应后溶液中n(H+)=2mol
c(H+)=$\frac{2mol}{0.5L}$=4mol/L,
答:溶液中H+的物质的量浓度为4mol/L.
点评 本题考查化学方程式的计算,题目难度不大,注意根据反应的化学方程式计算.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2017届江西省高三上第二次月考化学试卷(解析版) 题型:选择题
用二氧化氯(ClO2)新型净水剂替代传统的净水剂Cl2,对淡水进行消毒是城市饮用水处理的新技术,其中纤维素还原法制ClO2是一种新方法,其原理是:纤维素水解得到的最终产物与NaClO3反应生成ClO2。则消耗1mol最终产物转移电子的物质的量为
A.6mol B.20mol C.12 mol D.24mol
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该物质的名称为 2,2,3-三甲基-3-丁烯 | |
| B. | 分子中最多 4 个碳原子共平面 | |
| C. | 此物质转化为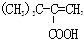 的过程中需依次经过加成、取代、氧化、消去反应 的过程中需依次经过加成、取代、氧化、消去反应 | |
| D. | 此物质与氢气加成后的产物与此物质中氢原子的种类数不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由于浓度差产生放热 | B. | 发生了水分解反应 | ||
| C. | 发生了盐分解反应 | D. | 盐的溶解程度增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不能用手直接接触药品 | B. | 可用酒精灯对烧杯直接加热 | ||
| C. | 用鼻孔凑到容器口去闻气体的气味 | D. | 尝一下实验室里酒精的味道 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
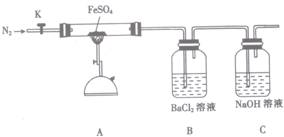
| 操作步骤 | 实验现象 | 用化学方程式解释原因 |
| 打开K,通入一段时间的N2,关闭活塞K,加热A中的玻璃管一段时间 | 洗气瓶B中①有白色沉淀生成 | ②SO3+H2O+BaCl2=BaSO4↓+2HCl |
| A中固体不再分解后,停止加热,打开K,缓慢通入氮气至玻璃管冷却 | 硬质玻璃管中最终可以看到③有红棕色固体物质生成 | ④2FeSO4$\frac{\underline{\;高温\;}}{\;}$Fe2O3+SO2↑+SO3↑ |
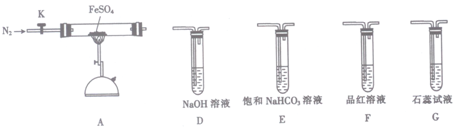
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O2、Na2O2都属于过氧化物,都存在共价键 | |
| B. | 双氧水是绿色氧化剂,可作医疗消毒剂 | |
| C. | H2O2既有氧化性,又有还原性,与Cl2、KMnO4反应是表现H2O2的氧化性 | |
| D. | H2O2做漂白剂是利用其氧化性,漂白原理与HClO类似,与SO2不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.12升 | B. | 2,24升 | C. | 2.94升 | D. | 5.88升 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com