
【题目】将浓度均为0.5molL-1氨水和KOH溶液分别滴入到体积均为20mL且浓度相同的AlCl3溶液中,测得溶液的导电率与加入碱的体积关系如图所示,下列说法中错误的是( )

A.AlCl3溶液的物质的量浓度为0.2molL-1
B.根据图象可以确定导电率与离子种类有关
C.cd段发生的反应是Al(OH)3+OH-=AlO2-+2H2O
D.e点时溶液中的离子浓度:c(K+) =c(Cl-) +c(AlO2-)
【答案】D
【解析】
根据图象得出I为氨水滴加到氯化铝溶液中的图象,II为KOH滴加到氯化铝溶液中的图象,c点为恰好反应生成氢氧化铝沉淀的点。
A选项,根据分析得到c点恰好反应完生成氢氧化铝沉淀,氢氧化钾的物质的量是氯化铝物质的量的3倍,因此AlCl3溶液的物质的量浓度为 ,故A正确;
,故A正确;
B选项,根据图象可以确定导电率与离子种类、离子浓度有关,故B正确;
C选项,c点是氢氧化铝沉淀,再加入KOH,则沉淀开始溶解,其cd段发生的反应是Al(OH)3+OH-=AlO2-+2H2O,故C正确;
D选项,e点是KOH、KAlO2、KCl,溶液中的离子浓度:c(K+)+c(H+)=c(Cl-)+c(OH-)+c(AlO2-),故D错误。
综上所述,答案为D。


 小学教材全测系列答案
小学教材全测系列答案科目:高中化学 来源: 题型:
【题目】X(s)+3Y(g)![]() Z(g) ΔH=-a kJ·molˉ1 ,一定条件下,将2mol X和2 mol Y通入2L的恒容密闭容器中,反应10s,测得生成0.5molZ。下列说法正确的是
Z(g) ΔH=-a kJ·molˉ1 ,一定条件下,将2mol X和2 mol Y通入2L的恒容密闭容器中,反应10s,测得生成0.5molZ。下列说法正确的是
A.10s内,X的平均反应速率为0.025 mol·Lˉ1·sˉ1
B.第10s时,Y的反应速率为0.075 mol·Lˉ1·sˉ1
C.第10s时,X为 1.5 mol,Y的浓度为0.25 mol·Lˉ1
D.10s内,X和Y反应放出的热量为a kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如图所示(图中有些反应的生成物和反应的条件没有标出)。
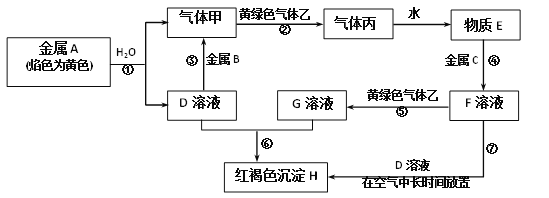
请根据以上信息完成下列各题:
(1)写出下列物质的化学式:B__________、丙__________。
(2)写出黄绿色气体乙的一种用途________________,反应过程⑦可能观察到的实验现象是_________________。
(3)写出反应①的化学方程式,并用单线桥法标出电子转移的方向和数目:______。
(4)反应③中的氧化剂是__________(写化学式,下同),反应④中的还原剂是________。
(5)写出反应⑤的离子方程式______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NaOH溶液吸收烟气中的SO2,将所得的吸收液用三室膜电解技术处理,原理如图所示.下列说法错误的是

A.电极a为电解池阴极
B.阳极上有反应HSO3—-2e—+H2O=SO42—+3H+发生
C.当电路中通过1mol电子的电量时,理论上将产生0.5mol H2
D.处理后可得到较浓的H2SO4和NaHSO3产品
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CoCl2·6H2O是一种饲料营养强化剂。以含钴废料(含少量Fe、Al等杂质)制取CoCl2·6H2O的一种新工艺流程如下图:
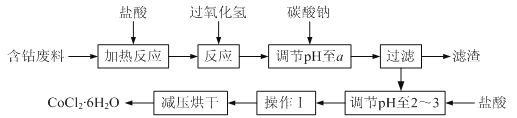
已知:①CoCl2·6H2O熔点86℃,易溶于水、乙醚等;常温下稳定无毒,加热至110~120℃时,易失去结晶水变成有毒的无水氯化钴。(乙醚:无色液体,沸点34.5℃,在水中的溶解度小)
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
开始沉淀 | 2.3 | 7.5 | 7.6 | 3.4 |
完全沉淀 | 4.1 | 9.7 | 9.2 | 5.2 |
请回答下列问题:
(1)钴的性质与铁相似,能与盐酸和硝酸反应,写出钴与盐酸反应的化学方程式:________________________________。
(2)在上述新工艺中,用“盐酸”代替原工艺中“盐酸与硝酸的混酸”直接溶解含钴废料,其主要优点:
①为__________________________,防止大气污染;
②防止产品中混有硝酸盐。
(3) 加入碳酸钠调节pH至a,a的范围应是5.2~_________。
(4) 操作Ⅰ包含3个基本实验操作,它们是蒸发浓缩、冷却结晶和_________。
(5)根据表中数据,判断Ksp[Fe(OH)3] ________Ksp[Co(OH)2] (填“<”、“=”或“>”) 。在实验室中,为了从上述产品中获得纯净的CoCl2·6H2O,采用的方法是:将产品溶于乙醚过滤后,再蒸馏。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖由来自美、英、日的三人分获,以表彰他们在锂离子电池研究方面做出的贡献,他们最早发明用LiCoO2作离子电池的正极,用聚乙炔作负极。回答下列问题:
(1)基态Co原子价电子排布图为______________(轨道表达式)。第四电离能I4(Co)比I4(Fe)小,是因为_____________________。
(2)LiCl的熔点(605℃)比LiF的熔点(848℃)低,其原因是_________________________.
(3)乙炔(C2H2)分子中δ键与π键的数目之比为_______________。
(4)锂离子电池的导电盐有LiBF4等,碳酸亚乙酯( )是一种锂离子电池电解液的添加剂。
)是一种锂离子电池电解液的添加剂。
①LiBF4中阴离子的空间构型是___________;与该阴离子互为等电子体的分子有_____________。(列一种)
②碳酸亚乙酯分子中碳原子的杂化方式有_______________________。
(5)Li2S是目前正在开发的锂离子电池的新型固体电解质,其晶胞结构如图所示,已知晶胞参数a=588pm。

①S2-的配位数为______________。
②设NA为阿伏加德罗常数的值,Li2S的晶胞密度为____________(列出计算式)![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气净化器中发生的反应为2NO(g)+2CO(g)![]() N2(g)+2 CO2(g)。一定温度下, 在三个体积均为1.0L恒容密闭容器中发生上述反应,测得有关实验数据如下:
N2(g)+2 CO2(g)。一定温度下, 在三个体积均为1.0L恒容密闭容器中发生上述反应,测得有关实验数据如下:
容器 | 温度/(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | ||||
NO | CO | N2 | CO2 | N2 | CO2 | ||
I | 400 | 0.2 | 0.2 | 0 | 0 | 0.12 | |
II | 400 | 0.4 | 0.4 | 0 | 0 | ||
III | 300 | 0 | 0 | 0.1 | 0.2 | 0.075 | |
下列说法正确是
A. 该反应的ΔS<0、ΔH<0
B. 容器I中达到平衡所需时间2s,则v(N2)=0.06 molL-1·S-1
C. 达到平衡时,体系中c(CO)关系:c(CO,容器II)>2c(CO,容器I)
D. 若起始时向I中充入NO、CO、N2、CO2各0.1mol,开始时V正>V逆
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将固体NH4I置于密闭容器中,在一定温度下发生下列反应:
①NH4I(s)![]() NH3(g)+HI(g);②2HI(g)
NH3(g)+HI(g);②2HI(g)![]() H2(g)+HI(g)
H2(g)+HI(g)
达到平衡时,c(H2)=0.5mol·L-1,c(HI)=4mol·L-1,则此温度下,反应①的平衡常数为
A.9B.16C.20D.25
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水晶石是生产玻璃的原料,工业上回收水晶石废料(主要含SiO2,还含有CeO2、CaO、MgO、Na2O等)中的SiO2并富集稀土元素Ce(铈)元素的一种流程如下:

已知CeO2不溶于水,微溶于稀酸。
⑴玻璃工业上用SiO2、Na2CO3和CaCO3在高温下反应制普通玻璃(Na2O·CaO·6SiO2)的化学方程式为_______。
⑵“还原”时发生反应的离子方程式为______。
⑶“还原”时稀硫酸应适当过量,目的除保证反应充分进行及加快反应速率外,还有______。还原时控制其他条件一定,只改变反应的温度,所得SiO2产品的纯度如右图所示。超过70℃所得SiO2产品纯度下降的原因是_______。

⑷洗涤SiO2的方法是_______。
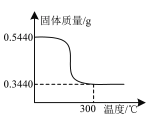
⑸向Ce2(SO4)3溶液中加入H2C2O4会析出Ce2(C2O4)3·10H2O晶体,将0.5440g Ce2(C2O4)3在N2气流中加热,所得残余固体的质量随温度的变化如图所示。已知加热时生成三种氧化物,写出Ce2(C2O4)3固体加热到300℃时反应的方程式:_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com