
Q、R、X、Y、Z为前20号元素中的五种,Q的低价氧化物与X单质分子的电子总数相等,R与Q同族,Y和Z的离子与Ar原子的电子层结构相同且Y的原子序数小于Z。
(1)Q的最高价氧化物,其固态属于____________晶体,俗名为____________。
(2)R的氢化物分子的空间构型是____________;属于________分子(填“极性”或“非极性”)它与X形成的化合物可作为一种重要的陶瓷材料,其化学式是____________。
(3)X的常见氢化物的空间构型是____________;它的另一氢化物X2H4是一种火箭燃料的成分,其电子式是____________。
(4)Q分别与Y、Z形成的共价化合物的化学式是________________和________________;Q与Y形成的分子的电子式是____________,属于____________分子(填“极性”或“非极性”)。
(1)分子 干冰
(2)正四面体 非极性 Si3N4
(3)三角锥形 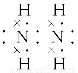
(4)CS2 CCl4 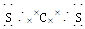 非极性
非极性
【解析】本题综合考查物质结构知识。根据题设条件可推知Q为C,R为Si,X为N,Y为S,Z为Cl。
(1)C的最高价氧化物为CO2,固态时是分子晶体,其俗名为干冰。
(2)Si的氢化物为SiH4,根据CH4的空间构型可知SiH4的空间构型为正四面体,SiH4分子中正负电荷重心重合,属于非极性分子。Si最外层有4个电子,N最外层有5个电子,它们形成化合物时,Si为+4价,N为-3价,其化学式为Si3N4。
(3)N的常见氢化物为NH3,其空间构型为三角锥形。根据N、H原子的成键原则,可得N2H4的结构简式为H2N—NH2,根据其结构简式可推写出其电子式。
(4)C与S可形成CS2,根据CO2的结构可写出CS2的电子式并知其为非极性分子。C与Cl形成CCl4分子。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014年高二鲁科选修3化学规范训练2.4分子间作用力物质性质练习卷(解析版) 题型:填空题
下图是Na、Cu、Si、H、C、N等元素单质的熔点高低的顺序,其中c、d均是热和电的良导体。

(1)请写出上图中d单质对应元素原子的电子排布式_________________________。
(2)单质a、b、f对应的元素以原子个数比1∶1∶1形成的分子中含__________个σ键,__________个π键。
(3)a与b的元素形成的10电子中性分子X的空间构型为__________;将X溶于水后的溶液滴入到含d元素高价离子的溶液中至过量,生成的含d元素离子的化学式为____________,其中X与d的高价离子之间以____________键结合。
(4)上述六种元素中的一种元素形成的含氧酸的结构为 ,请简要说明该物质易溶于水的原因________________________________。
,请简要说明该物质易溶于水的原因________________________________。
查看答案和解析>>
科目:高中化学 来源:2014年高二鲁科版选修3化学规范训练2章化学键分子间作用力练习卷(解析版) 题型:选择题
在硼酸[B(OH)3]分子中,B原子与3个羟基相连,其晶体具有与石墨相似的层状结构。则分子中B原子杂化轨道的类型及同层分子间的主要作用力分别是( )。
A.sp,范德华力 B.sp2,范德华力
C.sp2,氢键 D.sp3,氢键
查看答案和解析>>
科目:高中化学 来源:2014年高二鲁科版选修3化学规范训练2.3离子键配位键与金属键练习卷(解析版) 题型:选择题
下列物质中的离子键最强的是( )。
A.KCl B.CaCl2 C.MgO D.Na2O
查看答案和解析>>
科目:高中化学 来源:2014年高二鲁科版选修3化学规范训练2.2.1典型分子空间构型练习卷(解析版) 题型:选择题
下列分子中的碳原子采取sp2杂化的是( )。
A.C2H2 B.C2H4 C.C3H8 D.CO2
查看答案和解析>>
科目:高中化学 来源:2014年高二鲁科版选修3化学规范训练 3.3原子晶体与分子晶体练习卷(解析版) 题型:选择题
下列各组物质各自形成的晶体,均属于分子晶体的化合物的是( )。
A.NH3、HD、C10H8 B.PCl3、CO2、H2SO4
C.SO2、SiO2、P2O5 D.CCl4、Na2S、H2O2
查看答案和解析>>
科目:高中化学 来源:2014年高二鲁科版选修3化学规范训练 3.2金属晶体与离子晶体练习卷(解析版) 题型:选择题
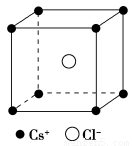
如图是CsCl晶体的晶胞结构(晶体中最小重复单元),已知晶体中两个最近的Cs+核间距离为a cm,氯化铯的式量为M,NA为阿伏加德罗常数,则氯化铯晶体的密度为( )。
A. 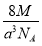 g·cm-3 B.
g·cm-3 B. 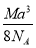 g·cm-3
g·cm-3
C. 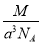 g·cm-3 D.
g·cm-3 D. 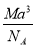 g·cm-3
g·cm-3
查看答案和解析>>
科目:高中化学 来源:2014年高二鲁科版选修3化学规范训练 2.1.2键参数练习卷(解析版) 题型:填空题
1919年,langmuir提出等电子原理:原子数相同、最外层电子总数相同的分子,互称为等电子体。等电子体的结构相似、物理性质相近。
(1)根据上述原理,仅由第二周期元素组成的共价分子中,互为等电子体的是:________和________;________和________。
(2)此后,等电子原理又有发展。例如:由短周期元素组成的物质中,与NO2-互为等电子体的分子有:__________、__________。
查看答案和解析>>
科目:高中化学 来源:2014年高二化学苏教版选修2 模块综合检测练习卷(解析版) 题型:选择题
下列有关新型高分子材料的说法中,不正确的是( )。
A.高分子分离膜应用于食品工业中,可用于浓缩天然果汁、乳制品加工和酿造业等
B.高吸水性树脂吸水量为自身质量的几十倍乃至上千倍,且既有吸水功能又有保水功能
C.导电塑料是应用于电子工业的一种新型高分子材料
D.合成高分子材料制成的人体器官一般都受到人体的排斥作用,难以达到生物相容的程度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com