
 2NH3 ,影响该反应速率的最主要因素( )
2NH3 ,影响该反应速率的最主要因素( )| A.浓度 | B.温度 | C.N2和H2的性质 | D.催化剂 |
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案科目:高中化学 来源:不详 题型:填空题
 Cl-+3 H+ +3 SO42-
Cl-+3 H+ +3 SO42-
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 xC(g);ΔH<0符合图象(Ⅰ)所示关系。由此推断对图象(Ⅱ)的不正确说法是(p3>p4)( )
xC(g);ΔH<0符合图象(Ⅰ)所示关系。由此推断对图象(Ⅱ)的不正确说法是(p3>p4)( )
| A.Y轴表示A的转化率 | B.Y轴表示B的质量分数 |
| C.Y轴表示混合气体的密度 | D.Y轴表示混合气体的平均相对分子质量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 5Ca2++3
5Ca2++3 +OH-
+OH-查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
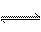 2Z(g):ΔH<0。降低温度时,对反应产生的影响是( )
2Z(g):ΔH<0。降低温度时,对反应产生的影响是( )| A.逆反应速率增大,正反应速率减小,平衡向逆反应方向移动 |
| B.逆反应速率减小,正反应速率增大,平衡向正反应方向移动 |
| C.正、逆反应速率都减小,平衡向正反应方向移动 |
| D.正、逆反应速率都增大,平衡向逆反应方向移动 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:多选题
A. | B. | C. | D. |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 编号 | 金属(粉末状)/mol | 酸的浓度及体积 | 反应温度/℃ |
| A | Mg,0.1 | 5mol/L盐酸10mL | 60 |
| B | Mg,0.1 | 3mol/L盐酸10mL | 60 |
| C | Fe,0.1 | 3mol/L盐酸10mL | 60 |
| D | Mg,0.1 | 3mol/L盐酸10mL | 50 |
| A.A | B.B | C.C | D.D |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 反应时间t(h) | 1 | 4 | 9 | 16 | 25 |
| MgO膜厚Y(nm) | 0.02a | 0.08a | 0.18a | 0.32a | 0.50a |
| ZnO膜厚Y(nm) | 1.0×10-3b | 4.0×10-3b | 9.0×10-3b | 1.6×10-2b | 2.5×10-2b |
| NiO膜厚Y(nm) | 0.3c | 0.6c | 0.9c | 1.2c | 1.5c |

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.温度 |
| B.溶液的浓度 |
| C.温度和溶液的浓度 |
| D.参加反应的各物质的性质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com