
��ͼ������A��M��һ�������µ�ת����ϵ�����ֲ��P��Ӧ����δ�г������ַ�Ӧ�ڹ�ҵ�����еõ�ʵ��Ӧ�á���֪��G�ǵ��ʣ��Ң���һ�ּ������ᷴӦ������Ӧ���������Ľ�����L��һ����ɫ���壬K��һ�ֺ���ɫ���壬E��һ�ֺ��ɫ������
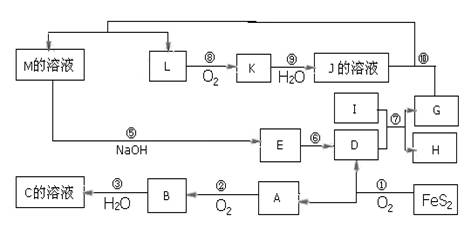
����д���пհף�
��1��д���������ʵĻ�ѧʽ��C�� ��J�� ��
��2��д�����з�Ӧ�Ļ�ѧ��Ӧ����ʽ��
��Ӧ�ߣ� ��
��Ӧ�⣺ ��
��3��д��ҵ��NH3��O2��һ����������ȡL�Ļ�ѧ����ʽ�� ��
��ÿ��2�֣���10�֣�����δд��һ�֣�
��1��C��H2SO4 J�� HNO3
��2����Ӧ�� �� Fe2O3
+ 2Al  Al2O3 + 2Fe
Al2O3 + 2Fe
��Ӧ�⣺Fe + 4HNO3 = Fe��NO3��3 +NO�� +2 H2O
��3��4NH3 + 5O2 4NO + 6H2O
4NO + 6H2O
��������
���������I�Ǽ�����ǿ�ᷴӦ��������������ǿ�Ӧ���������Ľ������ж�ΪAl��K��һ�ֺ���ɫ���壬�ж�ΪNO2��D������������ΪFe2O3����A���γ��������Ҫ����ΪSO2���ɷ�Ӧ4FeS2+11O2  2Fe2O3+8SO2֪A��DΪFe2O3��AΪSO2�����A+O2 ��B֪��AΪSO2��DΪFe2O3��BΪSO3��CΪH2SO4��I�Ǽ�����ǿ�ᷴӦ��������������ǿ�Ӧ���������Ľ���ΪAl��G��HΪAl2O3��Fe�е�һ�֣���K��һ�ֺ���ɫ���壬KΪNO2��JΪHNO3��LΪNO������G+HNO3 ��M+NO������֪GΪFe��HΪAl2O3��MӦΪFe��NO3��3��Fe��NO3��2����ϵ��Ӧ�ܣ�M+H2SO4 ��F+NO��֪��MΪFe��NO3��2��FΪFe��NO3��3��Fe2��SO4��3��EӦΪFe��OH��3������ȫ��������ȷ�����ֱ�Ϊ��A��SO2��B��SO3��C��H2SO4��D��Fe2O3��E��Fe��OH��3��F��Fe��NO3��3��Fe2��SO4��3��G��Fe��H��Al2O3��I��Al��J��HNO3��K��NO2��L��NO��M��Fe��NO3��2����Ŀ���漰�������˳�������
2Fe2O3+8SO2֪A��DΪFe2O3��AΪSO2�����A+O2 ��B֪��AΪSO2��DΪFe2O3��BΪSO3��CΪH2SO4��I�Ǽ�����ǿ�ᷴӦ��������������ǿ�Ӧ���������Ľ���ΪAl��G��HΪAl2O3��Fe�е�һ�֣���K��һ�ֺ���ɫ���壬KΪNO2��JΪHNO3��LΪNO������G+HNO3 ��M+NO������֪GΪFe��HΪAl2O3��MӦΪFe��NO3��3��Fe��NO3��2����ϵ��Ӧ�ܣ�M+H2SO4 ��F+NO��֪��MΪFe��NO3��2��FΪFe��NO3��3��Fe2��SO4��3��EӦΪFe��OH��3������ȫ��������ȷ�����ֱ�Ϊ��A��SO2��B��SO3��C��H2SO4��D��Fe2O3��E��Fe��OH��3��F��Fe��NO3��3��Fe2��SO4��3��G��Fe��H��Al2O3��I��Al��J��HNO3��K��NO2��L��NO��M��Fe��NO3��2����Ŀ���漰�������˳�������
��1����������������ƶϣ�A��������Ҫ�ɷ�Ϊ��SO2��A+O2��B��B+H2O��C����֪CΪH2SO4��DΪ����Fe2O3��EΪFe��OH��3��JΪHNO3��
��2����Ӧ�ߵĻ�ѧ����ʽΪ���ȷ�Ӧ����ѧ����ʽΪ��Fe2O3+2Al Al2O3+2Fe��
Al2O3+2Fe��
��Ӧ��ķ���ʽΪ��Fe + 4HNO3 = Fe��NO3��3 +NO�� +2 H2O��
��3�����ݽ̲�֪ʶ��д�䷽��ʽΪ4NH3 + 5O2 4NO + 6H2O��
4NO + 6H2O��
���㣺������ƶ�
���������⿼�����������������ת����ϵ������Ӧ�ã���Ҫ��������������з����ƶϸ����ʣ�ץס���ۢٺ������Ϣ����Ϸ�Ӧ��ת����ϵ�жϳ��������ǽ���ؼ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�


| ||
| ||
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�



| ||
| ||
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��8�֣���ͼ������A��M��һ�������µ�ת����ϵ�����ֲ��P��Ӧ����δ�г������У�I����Ȼ���к�����ߵĽ�����K��һ�ֺ���ɫ���塣
��1��A�� ��G�� ��
��2����Ӧ�ߵĻ�ѧ����ʽ�� ��
��3����Ӧ�ܵ����ӷ���ʽ�� ��
��4���ڷ�Ӧ�ڢۢޢ���,�����ڻ��Ϸ�Ӧ�����ڷ�������ԭ��Ӧ���� ��
��5����������D��KNO3��KOH���ڣ����Ƶ�һ�֡���ɫ��������Ч������K2FeO4��������أ���ͬʱ������KNO2��H2O���÷�Ӧ�Ļ�ѧ����ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013�����ʡ�����ظ���ѧ���������ο��Ի�ѧ�Ծ����������� ���ͣ������
��8�֣���ͼ������A��M��һ�������µ�ת����ϵ�����ֲ��P��Ӧ����δ�г��������У�I���ɵ�������Ԫ����ɵĵ������۵���ߵĽ����� K��һ�ֺ���ɫ���塣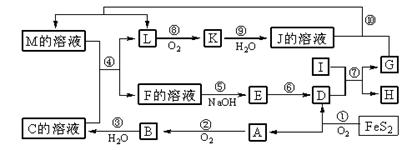
����д���пհף�
��1�������ڱ��У���ɵ���G��Ԫ��λ�ڵ�__________����_________�塣
��2���ڷ�Ӧ�����������뻹ԭ�������ʵ���֮��Ϊ ��
��3���ڷ�Ӧ�ڡ��ۡ��ޡ����У������ڻ��Ϸ�Ӧ�����ڷ�������ԭ��Ӧ���� ������д��ţ�
��4����Ӧ�ܵ����ӷ���ʽ�ǣ� ��
��5����������D��KNO3��KOH���ڣ����Ƶ�һ�֡���ɫ��������Ч��ˮ��K2FeO4��������أ���ͬʱ������KNO2��H2O���÷�Ӧ�Ļ�ѧ����ʽ�ǣ� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010�꽭��ʡ��һ�ڶ�ѧ�����п��Ի�ѧ��ʵ��ࣩ���� ���ͣ������
��8�֣���ͼ������A��M��һ�������µ�ת����ϵ�����ֲ��P��Ӧ����δ�г������У�I����Ȼ���к�����ߵĽ�����K��һ�ֺ���ɫ���塣

��1��A�� ��G�� ��
��2����Ӧ�ߵĻ�ѧ����ʽ�� ��
��3����Ӧ�ܵ����ӷ���ʽ�� ��
��4���ڷ�Ӧ�ڢۢޢ���,�����ڻ��Ϸ�Ӧ�����ڷ�������ԭ��Ӧ���� ��
��5����������D��KNO3��KOH���ڣ����Ƶ�һ�֡���ɫ��������Ч������K2FeO4��������أ���ͬʱ������KNO2��H2O���÷�Ӧ�Ļ�ѧ����ʽ�� ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com