
下面是用电子式表示某些物质的形成过程,其中正确的是
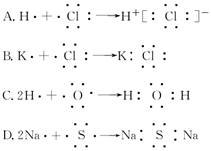
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源: 题型:





查看答案和解析>>
科目:高中化学 来源:浙江省东阳中学2009-2010学年高一下学期期中考试化学试题 题型:022
下图是元素周期表的部分框架,请回答:

(1)根据元素周期表回答下面问题:
a)元素周期表中的元素⑤和元素⑥的最高价氧化物的水化物中碱性较强是________(用分子式表示).周期表中的元素④和元素⑦的气态氢化物中沸点较高的是________(用结构式表示),理由是________.
b)元素①-⑦中的某单质在常温下化学性质稳定,通常可以做保护气的是________(用电子式表示).元素①和②形成的化合物,在工业制硝酸中催化氧化制NO,写出反应式________.
c)碳、氢、氧三种元素能形成许多种化合物,有些分子还会形成同分异构体,写出与乙醇(下图)互为同分异构体的有机化合物的结构式________
(2)元素周期表中位于斜对角线的两种元素及其性质十分相似,称之为对角线原则.根据元素周期表对角线原则,金属Be与铝单质及其化合物性质相似.
a)写出证明Al2O3是两性物质的化学反应的离子方程式:________,________.
b)Be(OH)2和Mg(OH)2可用试剂________鉴别.
查看答案和解析>>
科目:高中化学 来源:江苏省泰州中学2011-2012学年高一下学期期中考试化学试题 题型:022
下图是元素周期表的部分框架,请回答:
(1)根据元素周期表回答下面问题:
a)元素周期表中的元素⑤和元素⑥的最高价氧化物的水化物中酸性较强是________(用化学式表示).用电子式表示元素①与④的化合物的形成过程:________,该化合物属于________(填“共价”或“离子”)化合物.
b)元素①-⑦中的某单质在常温下化学性质稳定,通常可以做保护气的是________(用电子式表示).
c)碳、氢两种元素能形成许多种化合物,有些分子还会形成同分异构体.写出与己烷互为同分异构体,且一氯代物有两种的化合物的结构简式并命名________,________.
(2)元素周期表中位于斜对角线的两种元素及其性质十分相似,称之为对角线原则.根据元素周期表对角线原则,金属Be与铝单质及其化合物性质相似.
a)写出证明Al2O3是两性物质的化学反应的离子方程式:________,________.
b)Be(OH)2和Mg(OH)2可用试剂________鉴别.
查看答案和解析>>
科目:高中化学 来源:浙江省杭州十四中2012届高三9月月考化学试题 题型:022
| |||||||||||||||||||||||||||||
查看答案和解析>>
科目:高中化学 来源:2011-2012学年江苏省泰州中学高一下学期期中考试化学试卷(带解析) 题型:填空题
(18分)下图是元素周期表的部分框架,请回答:
| ① | | | | | | | | | | ||||||
| | | | | | | | ② | ③ | ④ | | |||||
| | | | ⑤ | ⑥ | | ⑦ | | ||||||||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com