
| A、Al3+、NO3-、K+、SO42ˉ |
| B、Ca2+、H+、CO32ˉ、AlO2- |
| C、OHˉ、SO42ˉ、NH4+、Al3+ |
| D、Fe3+、Mg2+、NO3ˉ、Clˉ |


科目:高中化学 来源: 题型:
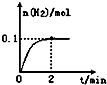 硫--碘循环分解水制氢主要涉及下列反应:
硫--碘循环分解水制氢主要涉及下列反应:查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | 相关信息知识 |
| A | 其原子的质量数=质子数=电子层数 |
| E | 原子核外有4个原子轨道填充了电子 |
| X | 其外围电子排布式为:nsnnp2n |
| Y | 地壳中含量最多的金属元素 |
| Z | 能形成多种氧化物,其中一种氧化物是具有磁性的黑色晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应后溶液中c(Na+)=2c(SO42-) | ||
B、
| ||
| C、沉淀的质量为49a g | ||
D、溶液中n(SO42-)=
|
查看答案和解析>>
科目:高中化学 来源: 题型:
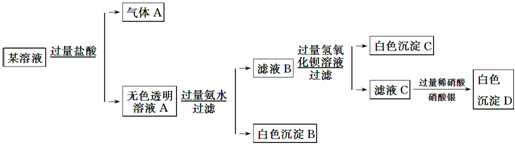
| A、原溶液中一定存在AlO2-、CO32-、SO42-、Cl-四种离子 |
B、气体A的化学式是CO2,其电子式为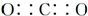 |
| C、原溶液中一定不存在的离子是Cu2+、Ba2+、Fe3+ |
| D、生成沉淀B的离子方程式为:Al3++3OH-=Al(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电解熔融氢氧化钠制钠,阴极发生电极反应为:Na++e-=Na |
| B、盖?吕萨克法制钠原理是利用铁的还原性比钠强 |
| C、若戴维法与盖?吕萨克法制得等量的钠,则两反应中转移的电子总数比为1:2 |
D、目前工业上常用电解熔融氯化钠法制钠(如图),电解槽中石墨极为阳极,铁为阴极 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硝酸钠晶体 |
| B、豆浆 |
| C、Fe (OH)3胶体 |
| D、75%的酒精溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com