
【题目】除去下列物质中含有的少量杂质(括号内为杂质),所选试剂不正确的是
A.Cl2(HCl):饱和食盐水、浓硫酸
B.AlCl3溶液(Fe3+):氨水、盐酸
C.C2H2(H2S):CuSO4溶液、碱石灰
D.NaCl溶液(SO42-):BaCO3、盐酸
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源: 题型:
【题目】纯的叠氮酸(HN3)是一种弱酸,常温下向25mL0.1mol/LNaOH溶液中加入0.2mol/LHN3溶液,滴加过程中的pH值的变化曲线(溶液混合时的体积变化忽略不计)如图。下列说法不正确的是( )
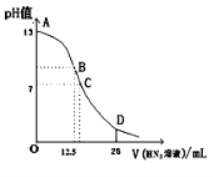
A.该滴定过程中应用酚酞作指示剂
B.若B点pH=8,则c(HN3)=(10-6-10-8)mol/L
C.沿曲线A→B→C的过程中,由水电离产生的c(OH-)逐渐减少
D.点D对应溶液中存在关系:c(N![]() )>c(Na+)>c(HN3)
)>c(Na+)>c(HN3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据如图判断,下列说法正确的是( )
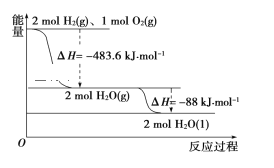
A. 氢气的燃烧热ΔH=-241.8 kJ·mol-1
B. 2 mol H2(g)与1mol O2(g)所具有的总能量比2 mol H2O(g)所具有的总能量低
C. 液态水分解的热化学方程式为2H2O(l)=2H2(g)+O2(g) ΔH=+571.6 kJ·mol-1
D. H2O(g)生成H2O(l)时,断键吸收的能量小于成键放出的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两个恒容的密闭容器中进行下列两个可逆反应:
甲:C(s)+H2O(g)![]() CO(g)+H2(g)
CO(g)+H2(g)
乙:CO(g)+H2O(g)![]() CO2(g)+H2(g)
CO2(g)+H2(g)
现有下列状态:①混合气体平均相对分子质量不再改变
②恒温时,气体压强不再改变 ③各气体组成浓度相等
④反应体系中温度保持不变 ⑤断裂氢氧键速率是断裂氢氢键速率的2倍 ⑥混合气体密度不变 ⑦单位时间内,消耗水蒸气质量与生成氢气质量比为9∶1
其中能表明甲、乙容器中反应都达到平衡状态的是( )
A. ①②⑤ B. ③④⑥ C. ⑥⑦ D. ④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚铜(CuCl)可用于冶金、电镀等行业,其制备的一种工艺流程如下:
I.溶解:取海绵铜(主要含Cu和CuO),加入稀硫酸和NH4NO3的混合溶液,控制溶液温度在60~70℃,不断搅拌至固体全部溶解,得蓝色溶液(过程中无气体产生);
II.转化:向蓝色溶液中加入(NH4)2SO3和NH4Cl,充分反应后过滤,得到CuCl粗品;
III.洗涤:CuCl粗品依次用pH=2硫酸和乙醇洗涤,烘干后得到CuCl产品。
(资料)CuCl固体难溶于水,与Cl-反应生成可溶于水的络离子[CuCl2]-;潮湿的CuCl固体露置于空气容易被氧化。
(1)过程I中:
①本工艺中促进海绵铜溶解的措施有________。
②氧化铜溶解的离子方程式是________。
③充分反应后NH4+的浓度约为反应前的2倍,原因是________。
(2)过程II中:
①(NH4)2SO3的作用是_________。
②NH4Cl的用量对铜的沉淀率的影响如下图所示。
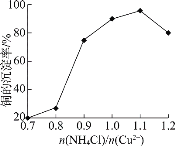
n(NH4Cl)/n(Cu2+)![]() 1.1时,CuCl的沉淀率下降的原因是________(用离子方程式表示)。
1.1时,CuCl的沉淀率下降的原因是________(用离子方程式表示)。
(3)过程III中,用乙醇洗涤的目的是________。
(4)产品纯度测定:量取CuCl产品a g于锥形瓶中,加入足量的酸性Fe2(SO4)3溶液使其充分溶解,然后用0.1000 mol/L KMnO4标准溶液滴定Fe2+,消耗KMnO4溶液b mL。(本实验中的MnO4-被还原为Mn2+,不与产品中杂质和Cl-反应)。
①CuCl溶于Fe2(SO4)3溶液的离子方程式是_________。
②产品中CuCl(摩尔质量为99g/mol)的质量分数为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期中8种元素a-h,其原子半径、最高正化合价或最低负化合价随原子序数递增的变化如图所示。
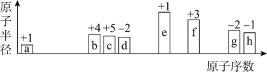
下列判断不正确的是
A.a、d、f组成的化合物能溶于强碱溶液
B.a可分别与b或c组成含10个电子的分子
C.e的阳离子与g的阴离子具有相同的电子层结构
D.最高价氧化物对应水化物的酸性:h>g>b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨基甲酸铵(H2NCOONH4)是一种氨化剂,易水解,难溶于CCl4。某小组设计下图所示装置制备氨基甲酸铵。已知:2NH3(g) + CO2(g)![]() H2NCOONH4(s) H<0。
H2NCOONH4(s) H<0。
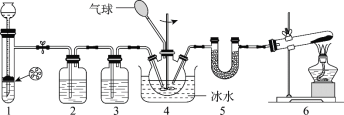
下列分析不正确的是
A.2中的试剂为饱和NaHCO3溶液
B.冰水浴能提高H2NCOONH4的产率
C.1和4中发生的反应均为非氧化还原反应
D.5中的仪器(含试剂)可用3中仪器(含试剂)代替
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验小组利用传感器探究Na2CO3和NaHCO3的性质。
实验操作 | 实验数据 |
测量下述实验过程的pH变化
|
|
下列分析不正确的是
A.①与②的实验数据基本相同,说明②中的OH-未参与该反应
B.加入试剂体积相同时,②所得沉淀质量大于③所得沉淀质量
C.从起始到a点过程中反应的离子方程式为:Ca2++2OH-+2HCO3-=CaCO3↓+2H2O+CO32-
D.b点对应溶液中水的电离程度小于c点对应溶液中水的电离程度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】尿素(![]() )氮原子上的氢原子可以像苯酚分子中苯环上的氢原子那样与甲醛发生反应,生成交联脲醛树脂,其结构片段如下图所示(图中 表示链延长)。
)氮原子上的氢原子可以像苯酚分子中苯环上的氢原子那样与甲醛发生反应,生成交联脲醛树脂,其结构片段如下图所示(图中 表示链延长)。
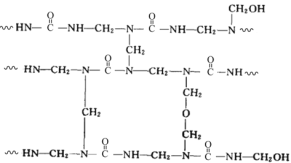
下列说法不正确的是
A.尿素可以与甲醛发生加成反应生成 ![]()
B.脲醛树脂的合成反应为缩聚反应
C.交联脲醛树脂在一定条件下可以发生水解反应,重新生成尿素和甲醛
D.甲醛可以与![]() 交联成网状结构的脲醛树脂
交联成网状结构的脲醛树脂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com