
【题目】甲、乙、丙、丁均为中学化学常见的纯净物,它们之间有如图所示的反应关系。下列物质组不满足上述转化关系的是
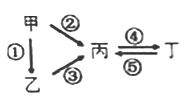
选项 | 甲 | 乙 | 丙 | 丁 |
A | Al | Al2O3 | NaAlO2 | Al(OH)3 |
B | S | H2S | SO3 | H2SO4 |
C | N2 | NH3 | NO | NO2 |
D | Si | SiO2 | Na2SiO3 | Na2CO3 |
A. A B. B C. C D. D
【答案】B
【解析】A、通过如下反应实现①Al+3O2![]() 2Al2O3(纯氧) ②Al2O3+2NaOH=2NaAlO2+H2O③2Al+2NaOH+2H2O=2NaAlO2+3H2↑④2NaAlO2+CO2+3H2O=2Al(OH)3↓+Na2CO3⑤Al(OH)3+NaOH=NaAlO2+2H2O;故A正确;B、①S+H2
2Al2O3(纯氧) ②Al2O3+2NaOH=2NaAlO2+H2O③2Al+2NaOH+2H2O=2NaAlO2+3H2↑④2NaAlO2+CO2+3H2O=2Al(OH)3↓+Na2CO3⑤Al(OH)3+NaOH=NaAlO2+2H2O;故A正确;B、①S+H2![]() H2S②2H2S +3O2 == 2SO2 + 2H2O③ S+O2
H2S②2H2S +3O2 == 2SO2 + 2H2O③ S+O2![]() SO2只生成SO2故B不能实现;C、通过如下反应实现①N2+3H2
SO2只生成SO2故B不能实现;C、通过如下反应实现①N2+3H2![]() 2NH3 ②4NH3+5O2
2NH3 ②4NH3+5O2![]() 4NO+6H2O③N2+O2
4NO+6H2O③N2+O2 ![]() 2NO④2NO+O2=2NO2⑤3NO2+H2O=2HNO3+NO,故C正确;D、通过如下反应实现①Si(粉)+O2
2NO④2NO+O2=2NO2⑤3NO2+H2O=2HNO3+NO,故C正确;D、通过如下反应实现①Si(粉)+O2![]() SiO2 ②SiO2+2NaOH=Na2SiO3+H2O③Si+2NaOH+H2O=Na2SiO3+2H2④Na2SiO3+H2O+CO2=Na2CO3+H2SiO3⑤Na2CO3+SiO2
SiO2 ②SiO2+2NaOH=Na2SiO3+H2O③Si+2NaOH+H2O=Na2SiO3+2H2④Na2SiO3+H2O+CO2=Na2CO3+H2SiO3⑤Na2CO3+SiO2![]() Na2SiO3+CO2,故D正确;故选B。
Na2SiO3+CO2,故D正确;故选B。


科目:高中化学 来源: 题型:
【题目】如图所示为向一定量AlCl3溶液中加入NaOH溶液后,产生Al(OH)3白色沉淀的质量与OH-的物质的量之间的关系曲线。请回答下列问题:
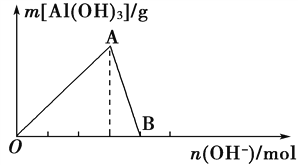
(1)A点时已参加反应的AlCl3和NaOH的物质的量之比为_______________________。
(2)OB段曲线所表示的反应,用一个离子方程式表示为____________________。
(3)向B处生成的溶液中通入过量二氧化碳,可观察到的现象是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的分类正确的是
碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 | |
A | NaOH | HCl | NaCl | Al2O3 | CO2 |
B | 纯碱 | H2SO4 | KMnO4 | CuO | SO2 |
C | KOH | HNO3 | NaHCO3 | Na2O | N2O5 |
D | 烧碱 | H2S | K2CO3 | CaO | NO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】质量分数为a%,物质的量浓度为c mol/L的KOH溶液,蒸发溶剂,恢复到原温度,若质量分数变为2a%,则物质的量浓度变为
A. 大于2c mol/L B. 等于 2c mol/L C. 小于2c mol/L D. 在 c mol/L~2c mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】七铝十二钙是新型的超导材料和发光材料,用白云石(主要含CaCO3和MgCO3)和废Al片制备七铝十二钙的工艺如下:
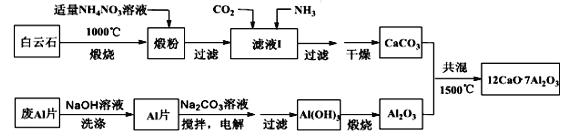
(1)煅粉主要含__________,该工艺中不能用(NH4)2SO4代替NH4NO3,原因是_________。
(2)滤液I中主要的阴离子有_________;若滤液I中仅通入CO2,会生成________,从而导致CaCO3产率降低。
(3)用NaOH溶液可除去废Al片表面的氧化膜,反应的离子方程式为______________。
(4)电解制备Al(OH)3时,电极分别为Al片和石墨,电解总反应方程式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的分类,正确的是( )
A. 烧碱、纯碱、熟石灰均属于碱
B. HCOOH、H2CO3、H2SO4均属于二元酸
C. 盐酸、BaSO4、NH3H2O均属于电解质
D. 酒精、冰水混合物、液氨均属于纯净物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某温度时CH3COOH的电离平衡常数为K。该温度下向20 mL 0.1 mol·L-1 CH3COOH溶液中逐滴加入0.1 mol·L-1 NaOH溶液,pH变化曲线如图所示(忽略温度),以下叙述正确的是
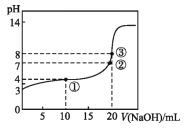
A.根据图中数据可计算出K值约为1×10-5
B.①②③点水的电离程度由大到小的顺序为:②>③>①
C.点①所示溶液中:c(CH3COO-)+c(OH-)=c(CH3COOH)+c(H+)
D.点③时c(CH3COOH)+c(CH3COO-)=0.1 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述错误的是( )
A.任何可逆反应都有一定的限度
B.化学反应达到平衡状态时,正、逆反应速率相等
C.化学反应达到平衡状态与时间的长短无关
D.化学平衡状态是不可改变的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向1L的密闭容器中加入1molX、3molZ和一定量的Y三种气体。一定条件下发生反应,各物质的浓度随时间变化如图一所示。图二为t2时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件。下列说法不正确的是
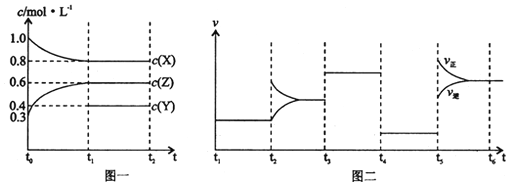
A. Y的起始物质的量为0.5mol
B. 该反应的化学方程式为:2X(g)+Y(g)![]() 3Z(g)ΔH<0
3Z(g)ΔH<0
C. 若t0=0,t1=10s,则t0-t1阶段的平均反应速率为v(z)=0.03mol/(L﹒s)
D. 反应物X的转化率t6点比t3点高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com