
下列关于混合物、纯净物、电解质和非电解质的正确组合是
纯净物 | 混合物 | 电解质 | 非电解质 | |
A | 盐酸[ | NaCl溶液 | 硫酸 | 干冰 |
B | 冰醋酸 | Fe(OH)3胶体 | 硫酸钡 | 二氧化硫 |
C | 石墨 | 空气 | 苛性钾 | 碳酸钙 |
D | 浓硫酸 | 氨水 | 氯化钠 | 氯气 |
科目:高中化学 来源:2015-2016学年福建省高一上学期期中考试化学试卷(解析版) 题型:填空题
现有下列物质:①碳酸钠 ②氧化钠 ③二氧化硅 ④铁 ⑤氧气 ⑥氢氧化钙 ⑦硫酸 请将上述物质按下列要求分类,并将其序号填入空白处:
(1)按组成分类,属于单质的是 ,属于氧化物的是 ,属于酸的是 ,属于碱的是 ,属于盐的是 。
(2)写出①分别与⑥、⑦在溶液中反应的离子方程式:___________________、___________________
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省高一上学期期中考试化学试卷(解析版) 题型:选择题
将钠、铁、铝各0.3 mol分别放入l00 mLl mol/L盐酸中,同温同压下产生气体的体积比是
A.1︰2︰3 B.6︰3︰2 C. 1︰1︰1 D.3︰1︰1
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高一上学期第二次月考化学试卷(解析版) 题型:选择题
下列物质种类中,前者包含后者的是
A.混合物 溶液 B.电解质 化合物 C.浊液 胶体 D.单质 化合物
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省简阳市高一上学期第三次月考化学试卷(解析版) 题型:实验题
现有下列化学仪器与用品:①玻璃棒 ②烧杯 ③托盘天平 ④量筒 ⑤药匙 ⑥胶头滴管 ⑦容量瓶 ⑧标签纸 ⑨细口试剂瓶
(1)称量:若需要配制460mL 0.1moL/L NaOH溶液,则应称取固体NaOH g;
(2)用以上称量后的NaOH固体配制溶液并备用:按配制溶液的过程顺序,从上述所给仪器和用品中选取需要的仪器(重复的不计),其编号排列是 ;
(3)配制过程中,应将固体NaOH溶解后并冷却至室温的溶液转移到 中;在液面接近容量瓶刻度线 处,改用 定容。
(4)若实验中遇到下列情况,可能导致溶液浓度偏高的是 (填字母):
A、固体氢氧化钠溶解时未冷却至室温,就开始转移、洗涤以及定容;
B、转移时不小心有少量溶液流到了容量瓶外;
C、定容时仰视容量瓶刻度线;
D、定容时加水超过了刻度线,马上用胶头滴管吸去多余的水。
E、配制好后,发现称量时所用的托盘天平的砝码生锈了
查看答案和解析>>
科目:高中化学 来源:2016届河北省高三上学期12月月考化学试卷(解析版) 题型:选择题
反应mA(s)+nB(g)  pC(g) ΔH<0,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,下列叙述中一定正确的是( )
pC(g) ΔH<0,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,下列叙述中一定正确的是( )
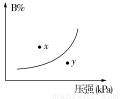
①m+n>p ②x点表示的正反应速率大于逆反应速率 ③n>p ④x点比y点时的反应速率慢 ⑤若升高温度,该反应的平衡常数增大
A.①②⑤ B.只有②④ C.只有①③ D.①③⑤
查看答案和解析>>
科目:高中化学 来源:2016届河南省开封市高三上学期第一次模拟理综化学试卷(解析版) 题型:选择题
NA代表阿伏伽德罗常数。已知C2H4和C3H6的混合物的质量为m g,则该混合物
A.所含碳原子总数为m NA/14
B.所含碳氢键数目为3m NA/14
C.所含公用电子对数目为(m/14+1)NA
D.完全燃烧时消耗的O2一定是33.6m/14 L
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省高二上第三次月考化学试卷(解析版) 题型:选择题
下列物质属于强电解质且能导电的是
①氯化钠溶液 ②氯化铵固体 ③铜 ④石墨 ⑤熔融的NaOH ⑥稀硫酸 ⑦乙酸
A.⑤ B.①②⑥ C.②⑤⑥⑦ D.①③④⑤⑥
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高一上第三次段考化学试卷(解析版) 题型:填空题
能源问题是人类社会面临的重大课题,甲醇是未来重要的能源物质之一。
(1)合成甲醇的反应为:CO(g)+2H2(g)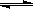 CH3OH(g);右图表示某次合成实验过程中甲醇的体积分数
CH3OH(g);右图表示某次合成实验过程中甲醇的体积分数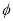 (CH3OH)与反应温度的关系曲线,则该反应的△H 0。(填“>、<或=”下同)
(CH3OH)与反应温度的关系曲线,则该反应的△H 0。(填“>、<或=”下同)

(2)若在230℃时,平衡常数K=1。若其它条件不变,将温度升高到500℃时,达到平衡时,K 1。
(3)在某温度下,向一个容积不变的密闭容器中通入2.5mol CO和7.5mol H2,达到平衡时CO的转化率为90%,此时容器内的压强为开始时的 倍。
(4)利用甲醇燃料电池设计如图所示的装置:
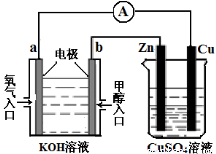
①则该装置中b为 极。
②当铜片的质量变化为12.8 g时,a极上消耗的O2 在标准状况下的体积为 L。
(5)低碳经济是以低能耗、低污染、低排放为基础的经济模式,其中一种技术是将CO2转化成有机物实现碳循环。如:
2CO2(g)+2H2O(l)== C2H4(g)+3O2(g) ΔH=+1411.0 kJ/mol
2CO2(g)+3H2O(l)== C2H5OH(1)+3O2(g) ΔH=+1366.8 kJ/mol
则由乙烯水化制乙醇反应的热化学方为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com