
N、O、Si、S是重要的非金属元素,下列说法正确的是
A.N、O、S、Si的原子半径逐渐增大,非金属性逐渐减弱
B.氮的氧化物和硫的氧化物既是形成光化学烟雾,又是形成酸雨的主要物质
C.S、SO2和Si、SiO2四种物质均能与NaOH溶液反应,各自又能与某些酸反应
D.N、Si、S的单质均能和氧气反应,生成的产物分别是NO2、SiO2和SO2
科目:高中化学 来源: 题型:
铊盐被列为A级危险品。铊(Tl)与铝同主族,原子序数为81,Tl3+与Ag在酸性介质中发生反应:Tl3+ +2Ag===Tl+ +2Ag+。已知Ag+ +Fe2+===Ag+Fe3+,下列推断正确的是
A.氧化性:Tl3+>Ag+>Fe3+ B.Tl + 最外层有3个电子
C.Tl(OH)3与Al(OH)3类似,都是两性氢氧化物 D.铊位于第五周期IIIA族
查看答案和解析>>
科目:高中化学 来源: 题型:
在2008年国际奥林匹克化学竞赛中,某兴趣小组在“探究卤素单质的氧化性”的实验中发现:在足量的稀氯化亚铁溶液中,加入1~2滴溴水,振荡后溶液呈黄色。
为此提出问题:Fe3+、Br2谁的氧化性更强?
(1)猜想
①澳大利亚代表团同学认为氧化性:Fe3+>Br2,故上述实验现象不是发生化学反应所致,则溶液呈黄色是含________(填化学式,下同)所致。
②美国代表团同学认为氧化性:Br2>Fe3+,故上述实验现象是发生化学反应所致,则溶液呈黄色是含________所致。
(2)设计实验并验证
为验证美国代表团同学的观点,选用下列某些试剂设计出两种方案进行实验,并通过观
察实验现象,证明了美国代表团同学的观点确实是正确的。
可以选用的试剂:a.酚酞试液;b.CCl4;c.无水酒精;d.KSCN溶液。
请你在下表中写出选用的试剂及实验中观察到的现象。(试剂填序号)
| 选用试剂 | 实验现象 | |
| 方案1 | ||
| 方案2 |
(3)结论
氧化性:Br2>Fe3+。故在足量的稀氯化亚铁溶液中,加入1~2滴溴水,溶液呈黄色所发生的离子反应方程式为________________________________________________
(4)依据上述结论,向FeBr2溶液中通入等量Cl2,写出该反应的离子方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
化学是一门以实验为基础的科学,化学实验是化学学习的重要内容。
(1)根据你掌握的知识,下列描述正确的是 (填序号)
①将0.2mo1·L-1FeC13溶液滴加沸水中,然后继续加热并不断搅拌可制得氢氧化铁胶体;
②将95g蒸馏水倒入盛有5g氯化钠的200ml的烧杯中,搅拌溶解,配制5%的食盐水;
③实验室配制氯化亚铁溶液时,将氯化亚铁先溶解在盐酸中,然后用蒸馏水稀释并加入少量铁粉
④使用容量瓶,滴定管、分液漏斗时,首先应检验仪器是否漏水;
⑤向某溶液中加入Ba(NO3)2溶液有白色沉淀产生,加盐酸沉淀不消失,则原溶液中一定含有SO42-。
(2)实验室中需要480ml0.4mo1·L-1CuSO4溶液,应称取硫酸铜晶体(CuSO4·5H2O)的质量是 g;所用仪器除托盘天平(带砝码)、量筒、烧杯、玻璃棒、药匙外,还缺少的玻璃仪器是 ;在观察液面定容时,若俯视刻度线,会使所配制的溶液的浓度 ;(填“偏高、偏低或无影响”下同) 转移溶液前容量瓶内有少量蒸馏水 ;
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的值,下列叙述正确的是
A.含有NA个氮原子的氮气在标准状况下的体积约为11.2L
B.25℃,1.01×105Pa,64gSO2中含有的原子数小于3NA
C.在常温常压下,11.2L Cl2含有的分子数为0.5NA
D.1 mo1 Na2O2与足量H2O反应,转移了2 NA 个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
A+B→X+Y+ H2O(为配平,反应条件略去)是中学常见反应的化学方程式,其中A、B的物质的量之比为1:4.请回答:
(1)若Y是黄绿色气体,该反应的化学方程式是 .
(2)若A为非金属单质,构成它的原子核外最外层电子数是次外层电子数的2倍,B的溶液为某浓酸,则反应中氧化剂与还原剂的物质的量之比是 .
(3)若A为金属单质,常温下A在B的浓溶液中“钝化”,且A可溶于X溶液中.
①A元素在周期表中的位置是______ (填所在周期和族);Y的化学式是______.
②含a mol X的溶液溶解了一定量A后,若溶液中两种金属阳离子的物质的量恰好相等,则被还原的X是______ mol.
(4)若A、B、X、Y均为化合物.A溶于水电离出的阳离子和水作用的生成物可净化水,向A溶液中加入硝酸酸化的AgNO3溶液,产生白色沉淀;B的焰色为黄色.则向A中逐滴加入B的离子方程式为
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验可行的是( )
|
| A. | 用澄清石灰水检验CO中含有的CO2 |
|
| B. | 用BaCl2除去NaOH溶液中混有的少量Na2SO4 |
|
| C. | 用KSCN溶液检验溶液中含有的Fe2+ |
|
| D. | 用溶解、过滤的方法分离CaCl2和NaCl固体混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示,下列判断中正确的是( )
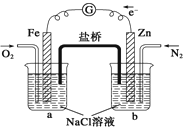
|
| A. | 烧杯a中的溶液H+增大 |
|
| B. | 烧杯b中发生氧化反应 |
|
| C. | 烧杯a中发生的反应为:2H++2e﹣═H2 |
|
| D. | 烧杯b中发生的反应为:2Cl﹣﹣2e﹣═Cl2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com