
| A. | H2SO4既不是氧化剂又不是还原剂 | |
| B. | 1molKClO3参加反应时有5mol电子转移 | |
| C. | KClO3是氧化剂 | |
| D. | 被氧化与被还原的氯元素的质量比为1:5 |
分析 5KCl+KClO3+3H2SO4═3Cl2↑+3K2SO4+3H2O中,Cl元素的化合价由-1价升高为0,Cl元素的化合价由+5价降低为0,该反应转移5e-,以此来解答.
解答 解:A.H、S、O元素的化合价不变,H2SO4既不是氧化剂又不是还原剂,故A正确;
B.1molKClO3参加反应时有1mol×(5-0)=5mol电子转移,故B正确;
C.KClO3中Cl元素的化合价降低,则是氧化剂,故C正确;
D.5个Cl失去电子与1个Cl得电子数目相等,则被氧化与被还原的氯元素的质量比为5:1,故D错误;
故选D.
点评 本题考查氧化还原反应,为高考高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念和转移电子的考查,题目难度不大.


科目:高中化学 来源: 题型:实验题
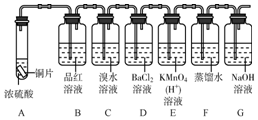 下面是某同学学习硫元素的学习方案.
下面是某同学学习硫元素的学习方案.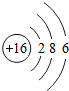 ,从结构知道硫元素是一种典型非金属元素.
,从结构知道硫元素是一种典型非金属元素.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.7克金属铝变为铝离子时失去的电子数目为0.3NA | |
| B. | 标准状况,0.5molN2含有的分子数为0.5NA | |
| C. | 在常温、常压下,1molHCl、H2O或I2所含有的分子数都为 NA | |
| D. | 在同温、同压下,相同物质的量的任何气体单质所含有的原子数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “滴水石穿,绳锯木断”不包含化学变化 | |
| B. | “天宫一号”中使用的碳纤维,是一种新型有机高分子材料 | |
| C. | 二氧化硅可用于光纤通信、单晶硅可用于光电转换 | |
| D. | 淀粉、油脂和蛋白质都是高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
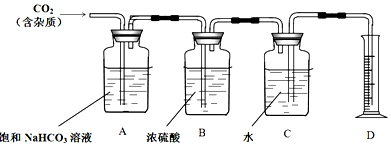
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 炭具有强还原性,高温下能将二氧化硅还原为硅 | |
| B. | 碳酸氢钠能与碱反应,可用作食品的蓬松剂 | |
| C. | 浓硫酸具有吸水性,可用于干燥氨气、二氧化碳等气体 | |
| D. | 铝能置换出氧化铁中的铁,钢铁工业利用铝热反应冶炼铁 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3$→_{催化剂△}^{O_{2}}$NO2$\stackrel{H_{2}O_{2}(aq)}{→}$HNO3 | |
| B. | 含2molHCl的浓盐酸$→_{△}^{总量MnO_{2}}$0.5molCl2$\stackrel{石灰石}{→}$0.25molCa(ClO)2 | |
| C. | 饱和NaCl溶液$\stackrel{NH_{3}.CO_{2}}{→}$NaHCO3$\stackrel{△}{→}$Na2CO3 | |
| D. | 海水$\stackrel{熟石灰}{→}$Mg(OH)2$\stackrel{稀盐酸}{→}$MgCl2(aq)$\stackrel{通电}{→}$Mg |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com