
[s1]
 |
(1)若A、B均为气体,在水溶液中反应生成正盐D,其中A是形成酸雨的主要物质。则D的化学式是 。B发生催化氧化反应的化学方程式是 。
(2)若A、B、D含有相同的金属元素,则此元素在元素周期表中的位置是 ,工业上制取该金属单质的化学方程式为: ,现将X滴入B的溶液中至过量,该过程发生的离子方程式为: 。
(3)若A为无色无味的气体,B为盐,且A、B、D三种物质含有相同元素,则A的电子式为: ,A与B溶液反应生成D的离子方程式为: 。
[s1]28.
科目:高中化学 来源: 题型:
 在如图所示的实验装置中,E为一张用淀粉、碘化钾和酚酞混合溶液润湿的滤纸,C,D为夹在滤纸两端的铂夹,X,Y分别为直流电源的两极.在A,B中充满KOH溶液后倒立于盛有KOH溶液的水槽中,再分别插入铂电极.切断电源开关S1,闭合开关S2,通直流电一段时间后,请回答下列问题:
在如图所示的实验装置中,E为一张用淀粉、碘化钾和酚酞混合溶液润湿的滤纸,C,D为夹在滤纸两端的铂夹,X,Y分别为直流电源的两极.在A,B中充满KOH溶液后倒立于盛有KOH溶液的水槽中,再分别插入铂电极.切断电源开关S1,闭合开关S2,通直流电一段时间后,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
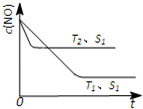 (2013?肇庆一模)消除汽车尾气是减少城市空气污染的热点研究课题.
(2013?肇庆一模)消除汽车尾气是减少城市空气污染的热点研究课题.查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

查看答案和解析>>
科目:高中化学 来源: 题型:
 如图所示装置中,C(Ⅰ)、C(Ⅱ)为多孔石墨电极,开始实验前两玻璃管(Ⅰ、Ⅱ)中盛满氢氧化钠溶液,且S1、S2均断开.先接通S1,两玻璃管中有气体生成(假设气体均未逸出装置),一段时间后,Ⅱ管中的气体体积是Ⅰ管中气体体积的2倍(两玻璃管中液面未脱离电极),再断开S1,接通S2,电流表的指针发生偏转.请回答:
如图所示装置中,C(Ⅰ)、C(Ⅱ)为多孔石墨电极,开始实验前两玻璃管(Ⅰ、Ⅱ)中盛满氢氧化钠溶液,且S1、S2均断开.先接通S1,两玻璃管中有气体生成(假设气体均未逸出装置),一段时间后,Ⅱ管中的气体体积是Ⅰ管中气体体积的2倍(两玻璃管中液面未脱离电极),再断开S1,接通S2,电流表的指针发生偏转.请回答:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
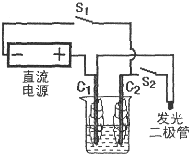 燃料电池是一种将化学反应产生的能量直接转换成电能的装置.某研究性学习小组在一次活动中,参照下图组装实验装置,以外面缠绕棉花的碳棒为电极,电解质溶液用0.5mol?L-1Na2SO4溶液,电源用3~6V直流电源,发光二极管起辉电压为1.7V,电流为0.6mA.
燃料电池是一种将化学反应产生的能量直接转换成电能的装置.某研究性学习小组在一次活动中,参照下图组装实验装置,以外面缠绕棉花的碳棒为电极,电解质溶液用0.5mol?L-1Na2SO4溶液,电源用3~6V直流电源,发光二极管起辉电压为1.7V,电流为0.6mA.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com