
反应mA(s)+nB(g)?eC(g)+fD(g),反应过程中, 当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图,下列叙述正确的是( )
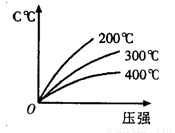
A.达到平衡后,加入催化剂则C%增大
B.达到平衡后,若升温,平衡左移
C.化学方程式中n<e+f
D.达到平衡后,增加A的量有利于平衡向右移动
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2016-2017学年河北省高二上学期第一次月考化学试卷(解析版) 题型:选择题
如图是工业上采用离子交换膜法电解足量饱和食盐水的示意图。下列有关说法中不正确的是( )

A.从E口逸出的是氢气
B.向B口中加入含少量NaOH的溶液以增强导电性
C.标准状况下每生成22.4 L Cl2,便产生2 mol NaOH
D.向电解后的阳极室溶液中加入适量盐酸,各物质可以恢复到电解前的浓度
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三上学期第一次段考化学卷(解析版) 题型:填空题
有五种可溶性物质A、B、C、D、E,它们所含的阴、阳离子互不相同,分别含有五种阳离子K+、Fe3+、Cu2+、Ba2+、Al3+和五种阴离子Cl-、OH-、NO3-、CO32-、X中的一种。
(1)某同学通过比较分析,认为无需检验就可判断其中必有的两种物质是_________和_________。
(2)物质C中含有离子X。为了确定X,现将(1)中的两种物质记为A和B,当C与A的溶液混合时,产生蓝色沉淀,向该沉淀中滴入稀HNO3,沉淀部分溶解,剩余白色固体,则X为 (填序号)。
A.Br- B.SO42- C.CH3COO- D.HCO3-
(3)将19.2gCu投入装有足量D溶液的试管中,Cu不溶解,再滴加稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现,写出Cu溶解的离子方程式 。
若要将Cu完全溶解,至少加入H2SO4的物质的量是 。
(4)E溶液与氢碘酸反应时可生成棕色物质,该反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上学期第一次月考化学试卷(解析版) 题型:填空题
甲醚(CH3OCH3)被称为21世纪的新型燃料,它清洁、高效、具有优良的环保性能,甲醚是一种无色气体,具有轻微的醚香味,其燃烧热为1455kJ/mol,甲醚可作燃料电池的燃料.
(1)写出甲醚 燃烧的热化学方程式 ;已知H2(g)和C(s)的燃烧热分别是285.8kJ·mol﹣1、393.5kJ·mol﹣1;计算反应4C(s)+6H2(g)+O2(g)═2CH3OCH3(g)的反应热为 ;
燃烧的热化学方程式 ;已知H2(g)和C(s)的燃烧热分别是285.8kJ·mol﹣1、393.5kJ·mol﹣1;计算反应4C(s)+6H2(g)+O2(g)═2CH3OCH3(g)的反应热为 ;
(2)工业上利用H2和CO2合成二甲醚的反应如下:6H2(g)+2CO2(g)═CH3OCH3(g)+3H2O(g)△H<0
①一定温度下,在一个固定体积的密闭容器中进行该反应.下列能判断反应达到化学平衡状态的是 (选填编号)
a.c(H2)与c(H2O)的比值保持不变
b.单位时间内有2mol H2消耗时有1mol H2O生成
c.容器中气体密度不再改变
d.容器中气体压强不再改变
②温度升高,该化学平衡移动后到达新的平衡,CH3OCH3 的产率将 (填“变
的产率将 (填“变 大”、“变小”或“不变”,下同),混合气体的平均式量将 ;
大”、“变小”或“不变”,下同),混合气体的平均式量将 ;
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上学期第一次月考化学试卷(解析版) 题型:选择题
在不同情况下测得A(g)+3B(g)  2C(g)+2D(g)的下列反应速率,其中反应速率最大的是( )
2C(g)+2D(g)的下列反应速率,其中反应速率最大的是( )
A.υ(D)=0.4 mol·L-1·s-1 B.υ(C)=0.5 mol·L-1·s-1
C.υ(B)=0.6 mol·L-1·s-1 D.υ(A)=0.15 mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上学期第一次月考化学试卷(解析版) 题型:选择题
已知充分燃烧ag乙炔气体生成1mol二氧化碳气体和液态水,并放出热量bkJ,则乙炔燃烧的热化学方程式正确的是( )。
A.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)ΔH=-4bkJ?mol-1
B.C2H2(g)+5/2O2(g)=2CO2(g)+H2O(l)ΔH=2bkJ?mol-1
C.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)ΔH=-2bkJ?mol-1
D.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)ΔH=bkJ?mol-1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省高二上学期9月月考化学试卷(解析版) 题型:填空题
镉镍可充电电池在现代生活中有着广泛的应用,它的充、放电反应如下:
Cd+2NiOOH+2H2O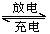 Cd(OH)2+2Ni(OH)2
Cd(OH)2+2Ni(OH)2
请回答下列问题:
(1)上述反应式中左边物质的总能量________(填“大于”“小于”或“等于”)右边物质的总能量。
(2)放电时负极发生反应的物质是________ ,
正极的电极反应式为__________________ 。
(3)镉镍废旧电池必须进行回收并集中处理,最主要的原因是____________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省咸宁市高二上学期第一次月考化学试卷(解析版) 题型:填空题
研究NOx、SO2、CO等大气污染气体的处理具有重要意义。
(1)已知:①CaCO3 (s)=CaO(s)+CO2 (g) △H= -180 kJ·mol-l;
②2CO(g)+SO2(g)=S(s)+2CO2 (g) △H= -270 kJ·mol-l
当反应②放出135 kJ热量时,处理的SO2质量为____________;若该反应放出的热量全部用于煅烧石灰石,则处理SO2时生成CO2与煅烧石灰石时生成的CO2的质量比为___________
(2)已知:CH4(g)+4NO2( g)=4NO(g)+CO2(g)+2H2O(g) △H= -560 kJ·mol-l;
CH4(g)+4NO(g)=2N2 (g)+CO2 (g)+2H2O(g) △H=-1160 kJ·mol-1;
① 若用标准状况下4.48 L CH4还原NO2生成N2,反应中转移的电子总数为_________,(用NA表示阿伏加德罗常数值),放出的热量为_________kJ。
②若1 mol CH4还原NO2时放出的热量为710 kJ,则生成的N2和NO的物质的量之比为____________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年北大附中河南分校高二上第一次月考化学卷(解析版) 题型:填空题
在2 L的密闭容器中进行反应:mX(g)+nY(g) == pZ(g)+qQ(g),式中m、n、p、q为化学计量数。在0~2 min内,各物质的物质的量变化如下表所示:
物质 | X | Y | Z | Q |
起始/mol | 0.7 | 1 | ||
2 min末/mol | 0.8 | 2.7[ | 0.8 | 2.7 |
已知2 min内v(Q)=0.075 mol·L-1·min-1,v(Z)∶v(Y)=1∶2。
(1)试确定以下物质的相关量:起始时n(Y)=________,n(Q)=________。
(2)方程式中m=________,n=________,p=________,q=________。
(3)用Z表示2 min内的反应速率为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com