��һ��������þ��ͭ�Ͻ���뵽ϡ������Һ�У�����ǡ����ȫ��Ӧ�����跴Ӧ�����л�ԭ����ȫ����NO����������Һ�м������ʵ���Ũ��Ϊ3mol/L��NaOH��Һ��������ȫ��������ɳ�����������ԭ�Ͻ����������5��1g���������й���������ȷ����
- A.
��ʼ����Ͻ����������Ϊ16��4g
- B.
�μӷ�Ӧ����������ʵ���Ϊ0��1mol
- C.
���ɳ�����ȫʱ����NaOH��Һ�����Ϊ100mL
- D.
����²���NO�����Ϊ22��4��
C
������������ݷ�Ӧ����ʽ���Եó������ij���Ϊ������þ��������ͭ�������������Ϊ���������������������ӵ�����֮�ͣ��ڽ���������ķ�Ӧ�н�����ʧ���ӵ����ʵ������������е�Ԫ�صĵõ��ӵ����ʵ���������������þ��������ͭ�Ļ�ѧʽ��֪�����������ӵ����ʵ������ڽ�����ʧ�������ʵ�����������ϵ��������������ʵ���Ϊ0.3mol��������������ʵ���Ϊ0.15mol���Ͻ��������ΧΪ3.6��9.6g��A��������ɵ�NO�����ʵ���Ϊ0.1mol����μӷ�Ӧ������Ϊ0.4mol��B�������Ϊ���������������ʵ���Ϊ0.3mol�����Ϊ100mL,C����ȷ��D�����NO���Ϊ2.24L��
���㣺���������������Ӧ�ļ��㡣
�����������������Ӧ��һ��Ҫ�������õ��ӵ�ʧ�غ㼰�����غ㶨������⣬���ڽ��ۺ��⡣
��ϰ��ϵ�д�
���ϰ��
��Ŀ�����л�ѧ
��Դ��
���ͣ���ѡ��
�������ʵı��淽���У��������
- A.
�����Ľ����ƴ����ú����
- B.
AgNO3��Һ�������ɫ�Լ�ƿ��
- C.
ˮ��������ڲ��������Լ�ƿ��
- D.
Ư�������ϴ��ܷ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ
��Դ��
���ͣ���ѡ��
������������ȷ����
- A.
Ϊ��ʹһЩ����ʳƷ��ɫ���ʺ죬�ɶ��һЩ��������
- B.
Ϊ��ʹӤ����ʳƷ��Ũ����Ȥ�����ǿ�����Ӥ��ʳƷ�м�������ɫ��
- C.
ʳ�μӵ��Ƿ�ֹ����ȱ����ӵ�Ӫ��ǿ��������Ԥ���ط��Լ�״����
- D.
֬���б���֬����ĺ���Խ�ߣ���Ӫ����ֵԽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ
��Դ��
���ͣ���ѡ��
�����й��Ȼ�ѧ����ʽ�������У���ȷ����(����)
- A.
��20.0 g NaOH��ϡ��Һ��ϡ������ȫ�кͣ��ų�28.7 kJ�����������ʾ�÷�Ӧ�к��ȵ��Ȼ�ѧ����ʽΪ NaOH(aq)+HCl(aq) =NaCl(aq)+H2O(l)��H��+57.4 kJ/mol
- B.
��֪C(ʯī��s) =C(���ʯ��s)��H��0������ʯ��ʯī�ȶ�
- C.
��֪2H2(g)+O2(g) =2H2O(g) ��H��-483.6 kJ/mol����H2ȼ����Ϊ241.8 kJ/mol
- D.
��֪2C(s)+2O2(g) =2CO2(g) ��H1,��2C(s)+O2(g) =2CO(g)��H2����H1����H2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ
��Դ��
���ͣ���ѡ��
���������в���ȷ����
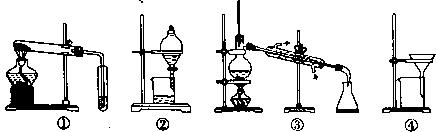
- A.
����װ�âټ���̼���ƺ�̼������
- B.
����װ�âڷ������ͺ�ˮ�Ļ����
- C.
����װ�â۽���ˮ����õ���ˮ
- D.
����װ�âܰѽ������Ӵӷ�ɢϵ�з������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ
��Դ��
���ͣ���ѡ��
������ʵ��˵��������������ʵ���
�ٴ�����Һ�ܵ��磻 �ڴ����ܺ�̼��Ʒ�Ӧ�ų�CO2��
�۳����£�0.1 mol/L�����pH��0.1 mol/L�����pH��
��0.1 mol/L��������ҺpHԼΪ9��
��ͬpH������ʹ�����������Ƭ��Ӧ���������H2��
- A.
�ڢۢ�
- B.
�ۢܢ�
- C.
�٢ۢ�
- D.
�ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ
��Դ��
���ͣ���ѡ��
������ɫ�ı仯�����˻�ѧ�������������йط�Ӧ����ɫ�仯��������������ˮ���ú����ɫ���ڵ�����Һ�����ʵ����ɫ�����廯������ֽ������ɫ�����ȵ�����ͭ���Ҵ�����ɫ������������Һ�͵⻯����Һ������������ɫ���ޱ����ڿ����б��������ۺ�ɫ��������ȷ����
- A.
�٢ڢܢݢ�
- B.
�ڢۢܢݢ�
- C.
�٢ڢۢܢ�
- D.
�٢ܢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ
��Դ��
���ͣ���ѡ��
����ʱ��ij��Һ����ˮ�������ɵ�H+��OH-���ʵ���Ũ�ȵij˻�Ϊ10-24�����ڸ���Һ��һ�����ܴ����������������
- A.
Al3+��Na+��NO3-��Cl-
- B.
K+��Na+��Cl-��CO32-
- C.
K+��Na+��Cl-��SO42-
- D.
NH4+��K+��SiO32-��NO3-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ
��Դ��
���ͣ���ѡ��
ʵ���ҳ�������ͭ��Һ���������е����⣺CuSO4+H2S��CuS��+H2SO4���÷�Ӧ�����Ʋ�
- A.
CuS��ˮ�⡡
- B.
CuS����������
- C.
��ͬ�¶��������ᱥ����Һ�������ӣ�S2-��Ũ�ȱ�CuS������Һ�д�
- D.
ǿ�������ȡ����
�鿴�𰸺ͽ���>>



 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
