
������25��ʱ�������ܵ���ʵ��ܽ�ȣ�
| ���ܵ���� | Mg(OH)2 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| �ܽ��/g | 9��12��4 | 1.7��12��6 | 1.5��12��4 | 3.0��12��9 |
������������ᴿ�У����������ܵ���ʵ��ܽ�ƽ��ԭ����ȥijЩ���ӡ����磺
��Ϊ�˳�ȥ�Ȼ���е�����Fe3�����Ƚ����������ˮ������һ�������Լ���Ӧ�����˽ᾧ
�� Ϊ�˳�ȥ�Ȼ�þ�����е�����Fe3�����Ƚ����������ˮ������������������þ����ַ�Ӧ�����˽ᾧ
�� Ϊ�˳�ȥ����ͭ�����е�����Fe2�����Ƚ����������ˮ������һ������H2O2����Fe2��������Fe3����������Һ��pH��4�����˽ᾧ
��ش��������⣺
��1�������������ӷ������ܹ��ﵽ�ܺ�Ч����Fe2����Fe3������ת��Ϊ ����ȥ
��2�����м�����Լ�Ӧ��ѡ��_________Ϊ�ˣ���ԭ����________________________��
��3�����г�ȥFe3�����������ܷ�Ӧ�����ӷ���ʽΪ_____________________________��
��4�������뷽������ص������У���ȷ����__________________������ĸ����
A��H2O2����ɫ�������������������в��������ʡ���������Ⱦ
B����Fe2������ΪFe3������Ҫԭ����Fe(OH)2������Fe(OH)3�������ѹ���
C��������ҺpH��4��ѡ����Լ���������ͭ���ʽ̼��ͭ
D��Cu2+���Դ���������pH��4����Һ��
E����pH>4����Һ��Fe3��һ�����ܴ�������
���𰸡���1������������2����ˮ�����������µ����ʣ�3��2Fe3����3Mg(OH)2 == 3 Mg2+ ��2Fe(OH)3 ��4��A C D E
������������������������������������ܽ��С����������Ҫ��PHֵ�ͣ�����ͨ����Fe2������ΪFe3��Ȼ���ٽ��г����������д����ܽ�ƽ�⣬���Ե������ܽ�ȸ�С�ij�����ʱ�������ᷢ��ת������Щ����������þʱ�ᷢ��������þ�ܽ����������������������������ʱһ�㲻�������µ����ʣ����Լ���ʱӦ�ü�������Һ����Ҫ������ͬ�������ӻ������ӣ�����Ϊ�˳�ȥ����ͭ�����е�����Fe2�����Ƚ����������ˮ������һ������H2O2����Fe2��������Fe3����Ȼ����Լ��뺬������ͭ��������ͭ������
���ɣ�
��1�����ó���ƽ��ʵ�ֳ���������ʱ������������Һ����Ҫ������ͬ�����ӵ���������д��������ȥ�Ȼ�þ�е������ӣ����Լ�������þ��������þ��̼��þ��̼����þ��
��2������ʱ���������µ��������ӣ��磺��Fe2������ΪFe3��ʱ��ֻ����H2O2��O3�ȣ�����Һ��ԭ�������ӣ������Կ�������ˮ�ȣ������ܼ�����Һ�в����е����ӡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��Է�������Ϊ100�������Һ���4������ͬ���칹�干�У������������칹�� ��������
A��3�� B��4�� C��5�� D��6��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���и������ʵ���ɫ��Һ�����������Լ����ɼ������ �� ��
��KOH Na2SO4 AlCl3 ��NaHCO3 Ba(OH)2 H2SO4
��HCl NaAlO2 NaHSO4 ��Ca(OH)2 Na2CO3 BaCl2
A���٢� B���ڢ� C���٢ۢ� D���٢ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ��ɫ����Һ����ȷ���Ƿ����������ӣ�Na+��Mg2+��Al3+��Fe2+��Ba2+��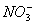 ��SO
��SO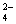 ��
��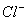 ��
��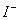 ��
��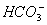 ��ȡ����Һʵ�����£�
��ȡ����Һʵ�����£�
| ʵ�鲽�� | ʵ������ |
| ��ȡ��������Һ���Ӽ��μ��� | ��Һ���ɫ |
| ��ȡ��������Һ��Ũ������CuƬ��ŨH2SO4������ | ����ɫ������������ڿ������ֱ�ɺ���ɫ |
| ��ȡ��������Һ����BaCl2��Һ | �а�ɫ�������� |
| ��ȡ�����ϲ���Һ����AgNO3��Һ | �а�ɫ�������ɣ��Ҳ�����HNO3 |
| ��ȡ��������Һ����NaOH��Һ | �а�ɫ�������ɣ���NaOH����ʱ���������ܽ� |
��1����Һ�п϶����ڵ�������________________________��
��2����Һ�п϶������ڵ�������________________________��
��3��Ϊ��һ��ȷ���������ӣ�Ӧ�ò����ʵ����________ _ ________
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ܴٽ�ˮ�ĵ��룬��ʹ��Һ��C(H+)>C(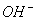 )�IJ����� �� ��
)�IJ����� �� ��
��1����ˮ������� ��2����ˮ��Ͷ��һС������� ��3����ˮ��ͨCO2 ��4����ˮ��ͨ
NH3 ��5����ˮ�м����������� ��6����ˮ�м���NaHCO3���� ��7����ˮ�м�NaHSO4����
A.��1����3����6����7�� B.��1����3����6�� C.��5����7�� D.��5��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����������ȷ����
A. 0.1 mol/LC6H5ONa��Һ�У�c(Na+)��c(C6H5O-)��c(H+)��c(OH-)
B. Na2CO3��Һ��ˮϡ�ͺָ���ԭ�¶ȣ�pH��Kw����С
C. pH=5��CH3COOH��Һ��Ph=5��NH4Cl��Һ�У�c(H+)�����
D. ��Na2S��Һ�м���AgCl���壬��Һ��c(S2-)�½�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
Fe(OH)3������ˮ������ƽ�⣺Fe��OH��3 Fe3++3
Fe3++3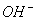 ����Fe(OH)3�������м��������������ʺ�ʹ��Һ�е�Fe3+Ũ���������
����Fe(OH)3�������м��������������ʺ�ʹ��Һ�е�Fe3+Ũ���������
A��NaOH��Һ B��ϡHCl C��ϡHI D��ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����£�AgCl��AgBr��AgI���ܶȻ�������Ksp������Ϊ1.8��12-12mol2��L-2��5.0��12-13mol2��L-2��8.3��12-17mol2��L-2�������й�˵��������� �� ��
A����������ˮ���ܽ�����AgCl>AgBr>AgI
B����AgCl����Һ�м�������ŨNaBr��Һ��AgBr��������
C����AgBr������Һ�м�������ŨNaCl��Һ��������AgCl��������
D����AgI����Һ�м���NaI������AgI��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��10 L�ܱ������У�1 mol A��3 mol B��һ�������·�Ӧ��A(g)��xB(g)  2C(g)��
2C(g)��
2 min��ﵽƽ�⣬����0.4 mol C����û�����干3.4 mol�������н����ȷ����
A��ƽ��ʱ�����ʵ���֮��n(A)��n(B)��n(C)��2��11��4
B��xֵ����3
C��A��ת����Ϊ20%
D��B��ƽ����Ӧ����Ϊ0.4 mol/(L��min)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com