
��15�֣�
��6�֣�����������ɶ�����̼��ˮ�ϳ������ǣ�ͬʱ�ų����������뽫�÷�Ӧ������������Ƴ�һ��ԭ��أ����������������ͽ�̫����ת����˵��ܡ�
��1��д����ԭ��ص��ܷ�Ӧʽ��______________________________________
��2��д���õ�������Խ����зŵ�ĵ缫��Ӧʽ��
������_____________________________________________
������_____________________________________________
��6�֣����˼ά��ѧϰ��ѧ����Ҫ������������Ƿ���ȷ���뾭�ܼ��顣�ڽ������˼ά��ʱ���ܻ�е��ȣ�һ��Ҫע��һЩ���ʵ������ԣ��Է�ֹ��ȳ�����Ľ��ۡ�ƾ���еĻ�ѧ֪ʶ��������Ƚ����ȷ���ǣ��������ţ� �������������д����ȷ�ġ�
������ͬ�����£�Na2CO3�ܽ�ȱ�NaHCO3��
��ȣ�����ͬ�����£�CaCO3�ܽ�ȱ�Ca��HCO3��2��
��ȷ��Ӧ��Ϊ���������ȷ���˴���д����ͬ������ ��
������������Һ��ͨ����CO2��CO2 +ClO- + H2O = HCO3- + HClO
��ȣ������������Һ��ͨ����SO2��SO2 + ClO- + H2O= HSO3- + HClO
��ȷ��Ӧ��Ϊ�� ��
�۸��ݻ��ϼ�Fe3O4�ɱ�ʾΪ��FeO��Fe2O3 ��ȣ�Fe3I8Ҳ�ɱ�ʾΪFeI2��2FeI3
��ȷ��Ӧ��Ϊ�� ��
��CaC2��ˮ�⣺CaC2+2H2O =Ca��OH��2 + C2H2��
��ȣ�Al4C3Ҳ��ˮ�⣺Al4C3 + 12H2O = 4Al��OH��3��+ 3CH4��
��ȷ��Ӧ��Ϊ�� ��
�����֣������£�ijˮ��ҺM�д��ڵ������У�Na+��A-��H+��OH-��������ҺM�� pH=3��HA��Һ![]() mL��pH=11��NaOH��Һ
mL��pH=11��NaOH��Һ![]() mL��Ϸ�Ӧ���ã�������˵������ȷ���� ������ĸ����
mL��Ϸ�Ӧ���ã�������˵������ȷ���� ������ĸ����
A������ҺM�����ԣ�����ҺM��C��H+��+C��OH-��=2��10-7mol��L-1
B����V1=V2������ҺM��pHһ������7
C������ҺM�����ԣ���V1һ������V2
D������ҺM�ʼ��ԣ���V1һ��С��V2

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����

| c(CH3CH2OH)?c(H2O) |
| c2(CO)?c4(H2) |
| c(CH3CH2OH)?c(H2O) |
| c2(CO)?c4(H2) |
| �¶ȣ�K�� CO2ת���ʣ�%�� n��H2��/n��CO2�� |
500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2 | 60 | 43 | 28 | 15 |
| 3 | 83 | 62 | 37 | 22 |
| n(H2) |
| n(CO2) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011�콭��ʡӥ̶�и����ڶ���ģ�⿼�����ۻ�ѧ���� ���ͣ���ѡ��
��15�֣�
��6�֣�����������ɶ�����̼��ˮ�ϳ������ǣ�ͬʱ�ų����������뽫�÷�Ӧ������������Ƴ�һ��ԭ��أ����������������ͽ�̫����ת����˵��ܡ�
��1��д����ԭ��ص��ܷ�Ӧʽ��______________________________________
��2��д���õ�������Խ����зŵ�ĵ缫��Ӧʽ��
������_____________________________________________
������_____________________________________________
��6�֣����˼ά��ѧϰ��ѧ����Ҫ������������Ƿ���ȷ���뾭�ܼ��顣�ڽ������˼ά��ʱ���ܻ�е��ȣ�һ��Ҫע��һЩ���ʵ������ԣ��Է�ֹ��ȳ�����Ľ��ۡ�ƾ���еĻ�ѧ֪ʶ��������Ƚ����ȷ���ǣ��������ţ� �������������д����ȷ�ġ�
������ͬ�����£�Na2CO3�ܽ�ȱ�NaHCO3��
��ȣ�����ͬ�����£�CaCO3�ܽ�ȱ�Ca��HCO3��2��
��ȷ��Ӧ��Ϊ���������ȷ���˴���д����ͬ������ ��
������������Һ��ͨ����CO2��CO2 + ClO- + H2O = HCO3- + HClO
��ȣ������������Һ��ͨ����SO2��SO2 + ClO- +H2O = HSO3- + HClO
��ȷ��Ӧ��Ϊ�� ��
�۸��ݻ��ϼ�Fe3O4�ɱ�ʾΪ��FeO��Fe2O3 ��ȣ�Fe3I8Ҳ�ɱ�ʾΪFeI2��2FeI3
��ȷ��Ӧ��Ϊ�� ��
��CaC2��ˮ�⣺CaC2+2H2O =Ca��OH��2 + C2H2��
��ȣ�Al4C3Ҳ��ˮ�⣺Al4C3 + 12H2O = 4Al��OH��3��+ 3CH4��
��ȷ��Ӧ��Ϊ�� ��
�����֣������£�ijˮ��ҺM�д��ڵ������У�Na+ ��A-��H+��OH-��������ҺM�� pH=3��HA��Һ
��A-��H+��OH-��������ҺM�� pH=3��HA��Һ mL��pH=11��NaOH��Һ
mL��pH=11��NaOH��Һ mL��Ϸ�Ӧ���ã�������˵������ȷ���� ������ĸ����
mL��Ϸ�Ӧ���ã�������˵������ȷ���� ������ĸ����
| A������ҺM�����ԣ�����ҺM��C��H+��+C��OH-��=2��10-7mol��L-1 |
| B����V1=V2������ҺM��pHһ������7 |
| C������ҺM�����ԣ���V1һ������V2 |
| D������ҺM�ʼ��ԣ���V1һ��С��V2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010-2011ѧ�꽭��ʡӥ̶�и����ڶ���ģ�⿼�����ۻ�ѧ���� ���ͣ�ѡ����
��15�֣�
��6�֣�����������ɶ�����̼��ˮ�ϳ������ǣ�ͬʱ�ų����������뽫�÷�Ӧ������������Ƴ�һ��ԭ��أ����������������ͽ�̫����ת����˵��ܡ�
��1��д����ԭ��ص��ܷ�Ӧʽ��______________________________________
��2��д���õ�������Խ����зŵ�ĵ缫��Ӧʽ��
������_____________________________________________
������_____________________________________________
��6�֣����˼ά��ѧϰ��ѧ����Ҫ������������Ƿ���ȷ���뾭�ܼ��顣�ڽ������˼ά��ʱ���ܻ�е��ȣ�һ��Ҫע��һЩ���ʵ������ԣ��Է�ֹ��ȳ�����Ľ��ۡ�ƾ���еĻ�ѧ֪ʶ��������Ƚ����ȷ���ǣ��������ţ� �������������д����ȷ�ġ�
������ͬ�����£�Na2CO3�ܽ�ȱ�NaHCO3��
��ȣ�����ͬ�����£�CaCO3�ܽ�ȱ�Ca��HCO3��2��
��ȷ��Ӧ��Ϊ���������ȷ���˴���д����ͬ������ ��
������������Һ��ͨ����CO2��CO2 + ClO- + H2O = HCO3- + HClO
��ȣ������������Һ��ͨ����SO2��SO2 + ClO- + H2O = HSO3- + HClO
��ȷ��Ӧ��Ϊ�� ��
�۸��ݻ��ϼ�Fe3O4�ɱ�ʾΪ��FeO��Fe2O3 ��ȣ�Fe3I8Ҳ�ɱ�ʾΪFeI2��2FeI3
��ȷ��Ӧ��Ϊ�� ��
��CaC2��ˮ�⣺CaC2+2H2O =Ca��OH��2 + C2H2��
��ȣ�Al4C3Ҳ��ˮ�⣺Al4C3 + 12H2O = 4Al��OH��3��+ 3CH4��
��ȷ��Ӧ��Ϊ�� ��
�����֣������£�ijˮ��ҺM�д��ڵ������У�Na+��A-��H+��OH-��������ҺM�� pH=3��HA��Һ mL��pH=11��NaOH��Һ
mL��pH=11��NaOH��Һ mL��Ϸ�Ӧ���ã�������˵������ȷ����
������ĸ����
mL��Ϸ�Ӧ���ã�������˵������ȷ����
������ĸ����
A������ҺM�����ԣ�����ҺM��C��H+��+C��OH-��=2��10-7mol��L-1
B����V1=V2������ҺM��pHһ������7
C������ҺM�����ԣ���V1һ������V2
D������ҺM�ʼ��ԣ���V1һ��С��V2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��̨��ʡ�߿����� ���ͣ���ѡ��


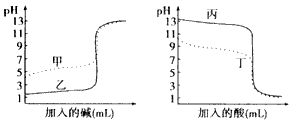

�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com