
【题目】I向KI和硫酸混合溶液中加入过氧化氢溶液,迅速反应放出大量气泡,溶液呈棕色.
查阅资料知,反应过程如下:
①H2O2+2KI+H2SO4=I2+K2SO4+2H2O;
②H2O2+I2=2HIO; ③H2O2+2HIO=I2+O2↑+2H2O
(1)用双线桥法表示过程①电子转移情况:H2O2+2KI+H2SO4=I2+K2SO4+2H2O
(2)上述实验过程②与③中,I2起到了的作用.
(3)试判断,酸性条件下HIO、H2O2、O2三种物质氧化性的强弱:(填化学式).
【答案】
(1)解: 
(2)催化剂
(3)H2O2>HIO>O2
【解析】解:(1)H2O2+2KI+H2SO4=I2+K2SO4+2H2O中O从﹣1价降低到﹣2价,I从﹣1价升高到0价,转移电子数为2,则用双线桥法表示电子转移为 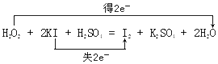 ;
;
故答案为:  ;(2)反应过程中,I2参与反应,最终又生成等量的I2 , 加快过氧化氢的分解,I2起催化剂作用,
;(2)反应过程中,I2参与反应,最终又生成等量的I2 , 加快过氧化氢的分解,I2起催化剂作用,
故答案为:催化剂;(3)由②H2O2+I2→2HIO,可知氧化性:H2O2>HIO,由③H2O2+2HIO→I2+O2↑+2H2O,可知氧化性:HIO>O2 , 故氧化性:H2O2>HIO>O2 ,
故答案为:H2O2>HIO>O2 .
(1)H2O2+2KI+H2SO4=I2+K2SO4+2H2O中O从﹣1价降低到﹣2价,I从﹣1价升高到0价,转移电子数为2;(2)反应过程中,I2参与反应,最终又生成等量的I2 , 加快过氧化氢的分解,I2起催化剂作用;(3)根据氧化性:氧化剂>氧化产物判断.


 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】《可再生能源法》倡导碳资源的高效转化及循环利用。下列做法与上述理念相违背的是
A. 加快石油等化石燃料的开采和使用 B. 大力发展煤的气化及液化技术
C. 以CO2 为原料生产可降解塑料 D. 将秸秆进行加工转化为乙醇燃料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列与实验相关的叙述正确的是( )
A.钠在氯气中燃烧,产生白色的烟雾
B.除去NaHCO3溶液中混有的少量Na2CO3,可加入适量的NaOH
C.配制溶液时,若加水超过容量瓶刻度,应该重新配制
D.检验某溶液是否含有SO42-时,应取少量该溶液,依次加入BaCl2溶液和稀盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有已知浓度的盐酸滴定未知浓度的NaOH溶液时,下列操作正确的是( )
A.滴定管用蒸馏水洗净后,直接加入已知浓度的盐酸
B.锥形瓶用蒸馏水洗净后,直接加入未知浓度的NaOH待测液
C.滴定前没有排出滴定管尖嘴处的气泡
D.读数时视线与滴定管内液体的凹液面最底处保持水平
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲组同学拟用高锰酸钾制取氧气,并收集和测量氧气体积,其装置如图所示. 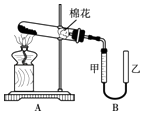
①读取装置B中收集到的气体体积时,需移动乙管与甲管中液面相齐,其目的是 .
②据报道高锰酸钾受热分解不产生MnO2 , 已知产气率= ![]() ×100%.若只发生KMnO4
×100%.若只发生KMnO4 ![]() KMnO2+O2↑,则产气率为 .
KMnO2+O2↑,则产气率为 .
③XRD谱显示还会分解产生K2MnO4和K2Mn4O8 , 写出分解产生这两种物质及氧气的化学方程式:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应属于取代反应的是( )
A.C2H4+3O2 ![]() ?2CO2+2H2O
?2CO2+2H2O
B.Zn+CuSO4═ZnSO4+Cu
C.NaCl+AgNO3═AgCl↓+NaNO3
D.CH2Cl2+Cl2 ![]() ?CHCl3+HCl
?CHCl3+HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制250mL0.10molL﹣1的NaOH溶液时,下列实验操作会使配得的溶液浓度偏大的是( )
A.转移溶液后未洗涤烧杯和玻璃棒就直接定容
B.所用NaOH已经潮解
C.带游码的天平称2.4gNaOH时误用了“左码右物”方法
D.在容量瓶中进行定容时俯视刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质性质与用途具有对应关系的是
A.SO2具有氧化性,可用于漂白纸浆
B.Si的熔点高,可用作半导体材料
C.FeCl3溶液显酸性,可用于蚀刻铜制的电路板
D.漂白液中含有强氧化性物质,可作漂白剂和消毒剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com