
分析 (1)充电是电解池,是将电能转化为化学能的装置,放电是原电池,阴离子移向负极;
(2)该电池工作时,铅蓄电池正极为PbO2,PbO2得电子发生还原反应,负极铅失电子发生氧化反应;
(3)Mg、Al和KOH溶液构成的原电池中,Al与KOH溶液反应失电子,Al作负极;
(4)酸性条件下,电池总反应为2H2+O2=2H2O,根据转移电子与反应物的关系2H2~4e-~O2计算.
解答 解:(1)充电是电解池,是将电能转化为化学能的装置,放电是原电池,阴离子移向负极,
故答案为:电;化学;负;
(2)该电池工作时,铅蓄电池正极为PbO2,PbO2得电子发生还原反应,电极反应为PbO2+SO42-+2e-+4H+═PbSO4+2H2O,负极铅失电子发生氧化反应,
故答案为:PbO2;PbO2+SO42-+2e-+4H+═PbSO4+2H2O;氧化;
(3)Mg、Al和KOH溶液构成的原电池中,Al与KOH溶液反应失电子,Al作负极,Mg作正极,负极反应为:Al-3e-+4OH-=AlO2-+2H2O,
故答案为:Al;Al-3e-+4OH-=AlO2-+2H2O;
(4)酸性条件下,电池总反应为2H2+O2=2H2O,转移电子与反应物的关系为:2H2~4e-~O2,外电路每流过4mol e-,消耗氢气的物质的量为2mol,氧气的物质的量为1mol,则消耗的气体在标况下共(2mol+1mol)×22.4L/mol=67.2L,
故答案为:67.2.
点评 本题考查原电池工作原理的应用,题目难度中等,注意把握电极方程式的书写方法,首先考虑原电池反应所依据的氧化还原反应,再考虑产物与电解质溶液的反应.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ①②③ | C. | ②③⑤ | D. | ②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业上可利用空气冷冻成液体后再分离来获得液氧 | |
| B. | 煤油燃烧后的主要产物是水和二氧化碳,绿色环保 | |
| C. | 煤油属于纯净物.主要成分是烃 | |
| D. | 火箭装载的燃料越多,说明其动力越大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4与Cl2的混合气体光照后颜色变浅 | |
| B. | 苯加入溴水中用力振荡,静止后水层变为无色 | |
| C. | C2H4通入酸性KMnO4溶液中,溶液紫色逐渐变浅 | |
| D. | C2H4通入Br2的CCl4溶液中,溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
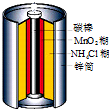
| A. | 电池内部含有电解质 | B. | 锌是负极,碳棒是正极 | ||
| C. | 电子由碳棒经外电路流向锌 | D. | 锌锰干电池属一次电池 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com