


 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
已知某溶液只存在OH- 、H+ 、NH4+、Cl-四种离子,某同学推测其离子浓度大小顺序可能有如下关系:
①c(Cl-)> c(NH4+) > c(H+) > c(OH-) ②c(NH4+) > c(OH-) > c(Cl-)>c(H+)
③c(NH4+) > c(Cl-)> c(OH-) >c(H+) ④c(Cl-)>c(H+)>c(NH4+) > c(OH-)
填写下列空白:
⑴若溶液中只有一种溶质,则该溶质是_________________,上述四种离子浓度的大小顺序(填序号)______________。
⑵若四种离子的关系符合③,则溶质为______________;若四种离子的关系符合④,则溶质为______________
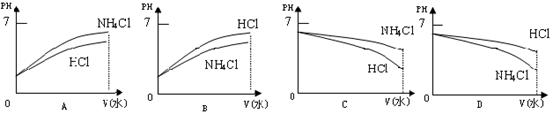
⑶将pH相同的溶液稀释相同的倍数,下面图像正确的是(填图像序号)______________。
⑷若该溶液是由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)_______c(NH3·H2O)(填“>”、“=”、“<”);混合前酸中c(H+)和碱中c(OH-)的关系为c(H+)_______c(OH-) (填“>”、“=”、“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
(14分)
现有A、B、C、D、E五种强电解质,分别含有下列阴阳离子(离子不可重复)。
| 阴离子 |
|
| 阳离子 |
|
已知:①A、B两溶液呈碱性,C、D、E溶液呈酸性。
②A、E两溶液反应既有气体,又有沉淀生成,A、C两溶液反应只有气体产生。
③D与其他四种溶液反应,均产生沉淀,C只与D反应产生沉淀。
试回答下列问题:
(1)写出:①B的化学式 ,②D与A反应生成难溶物的![]() 表达式 。
表达式 。
(2)A与E在溶液中反应的离子方程式为 。
(3)将pH相同的等体积A、B两种溶液稀释相同倍数后,溶液的pH关系是:![]()
![]() (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(4)将C溶液逐滴加入到等体积、等物质的量浓度的A溶液中,反应后溶液中各种离子浓度由大到小的顺序为 。
(5)在100mL 0.1![]() E溶液中,逐渐中入35 mL 2
E溶液中,逐渐中入35 mL 2![]()
![]() 溶液,最终得到沉淀的物质的量为 mol。
溶液,最终得到沉淀的物质的量为 mol。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年甘肃省兰大附中高二(上)期中化学试卷(解析版) 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com