


科目:高中化学 来源:浙江省宁波市八校2011-2012学年高二下学期期末联考化学试题 题型:013
|
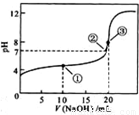
常温下,用0.10 mol·L-1 KOH溶液滴定10.00 mL 0.10 mol·L-1 H2C2O4(二元弱酸)溶液所得滴定曲线如图(混合溶液的体积可看成混合前溶液的体积之和).下列说法正确的是
| |
| [ ] | |
A. |
点①所示溶液中:c(H+)/c(OH-)=1012 |
B. |
点②所示溶液中:c(K+)+c(H+)=c(HC2O4-)+c(C2O42-)+c(OH-) |
C. |
点③所示溶液中:c(K+)>c(HC2O4-)>c(H2C2O4)>c(C2O42-) |
D. |
点④所示溶液中:c(K+)+c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.10 mol·L-1 |
查看答案和解析>>
科目:高中化学 来源:2015届浙江省高二上学期第一次质检化学试卷(解析版) 题型:选择题
常温下,用0.10 mol·L-1 KOH溶液滴定10.00 mL 0.10 mol·L-1H2C2O4(二元弱酸)溶液所得滴定曲线如图(混合溶液的体积可看成混合前溶液的体积之和)。下列说法正确的是( )

A.点①所示溶液中: c(H+)/c(OH—)=1012
B.点②所示溶液中:c(K+)+c(H+)=c(HC2O4—)+c(C2O42-)+c(OH—)
C.点③所示溶液中:c(K+)>c(HC2O4—)>c(H2C2O4)>c(C2O42-)
D.点④所示溶液中:c(K+)+ c(H2C2O4)+ c(HC2O4—) +c(C2O42-)=0.10mol·L-1
查看答案和解析>>
科目:高中化学 来源:2013-2014学年浙江省五校高三第一次联考化学试卷(解析版) 题型:选择题
常温下,用 0.10 mol·L-1 NaOH溶液分别滴定20.00 mL 0.10 mol·L-1 HCl溶液和20.00 mL 0.10 mol·L-1 CH3COOH溶液,得到2条滴定曲线,如下图所示,则下列说法正确的是( )


图1 图2
A.图2是滴定盐酸的曲线
B.a与b的关系是:a<b
C.E点对应离子浓度由大到小的顺序为: c(CH3COO-)> c(Na+)> c(H+)> c(OH-)
D.这两次滴定都可以用甲基橙作为指示剂
查看答案和解析>>
科目:高中化学 来源:2013届浙江省宁波市八校高二下学期期末联考化学试卷(解析版) 题型:选择题
常温下,用0.10 mol·L-1 KOH溶液滴定10.00 mL 0.10 mol·L-1H2C2O4(二元弱酸)溶液所得滴定曲线如图(混合溶液的体积可看成混合前溶液的体积之和)。下列说法正确的是

A.点①所示溶液中: c(H+)/c(OH—)=1012
B.点②所示溶液中: c(K+)+c(H+)=c(HC2O4—)+c(C2O42-)+c(OH—)
C.点③所示溶液中:c(K+)>c(HC2O4—)> c(H2C2O4)>c(C2O42-)
D.点④所示溶液中:c(K+)+ c(H2C2O4)+ c(HC2O4—) +c(C2O42-)=0.10mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,用 0.10 mol·L-1 NaOH 溶液分别滴定20.00 mL 0.10 mol·L-1 HCl溶液和20.00 mL 0.10 mol·L-1 CH3COOH溶液,得到2条滴定曲线,如下图所示:
 | |||
 |
图1 图2
则滴定HC1溶液的曲线是 _▲ (填“图1”或“图2”),说明判断依据 ▲ 。a与b的关系是:a _▲ b(填“>”、“<”或“=”);E点对应离子浓度由大到小的顺序为 _▲ ;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com