
| A、二氧化硅可用作半导体材料 |
| B、明矾可用于水的杀菌消毒 |
| C、碳酸氢钠可用于治疗胃酸过多 |
| D、硅可用于制造光导纤维 |


科目:高中化学 来源: 题型:
| A、3:1:1:1 |
| B、2:2:2:1 |
| C、1:2:2:1 |
| D、缺少条件,无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应温度必须控制在170℃ |
| B、反应物是乙醇和过量的3mol/L硫酸的混合液 |
| C、温度计应插入反应溶液液面以下 |
| D、反应容器中应加入少许瓷片 |
查看答案和解析>>
科目:高中化学 来源: 题型:
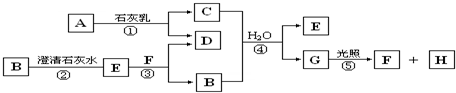
查看答案和解析>>
科目:高中化学 来源: 题型:
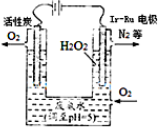 最近华南理工大提出利用电解法制H2O2并用产生的H2O2处理废氨水,装置如图
最近华南理工大提出利用电解法制H2O2并用产生的H2O2处理废氨水,装置如图查看答案和解析>>
科目:高中化学 来源: 题型:
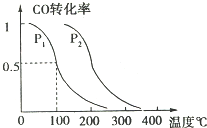 甲醇是一种可再生能源,具有广泛的开发和应用前景.
甲醇是一种可再生能源,具有广泛的开发和应用前景.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在NaHA溶液中一定有:c(Na+)>c(HA-)>c(OH-)>c(H+) |
| B、0.1mol/L(NH4)2Fe(SO4)2溶液中:c(SO42-)=c(NH4+)>c(Fe2+)>c(H+)>c(OH-) |
| C、0.2 mol?L-1CH3COOH溶液和0.2 mol?L-1CH3COONa溶液等体积混合:c(CH3COO-)+c(OH-)-c(H+)=0.1 mol?L-1 |
| D、pH相等的①NH4Cl ②(NH4)2SO4③NH4HSO4溶液中,c (NH4+)大小顺序为①=②>③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、升温 |
| B、加水 |
| C、加入NaOH溶液 |
| D、加入0.1mol/L HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com