
(11分)有关物质的量的计算。
(1)有NaCl、CaCl2、AlCl3三种溶液,若溶质的物质的量相等,分别与足量的硝酸银溶液反应,则生成沉淀的物质的量之比为________________.若生成的沉淀的质量相等,则三种溶液中溶质的物质的量之比为__________。
(2)相同质量的SO2和SO3,所含分子的数目之比为_________;所含O的物质的量之比为________。
(3)下列各物质所含原子数目,按由大到小顺序排列的是
①0.5mol NH3 ②标准状况下22.4L He ③4℃9mL水 ④0.2mol H3PO4
(1)1:2:3(2分);6:3:2(2分)
(2)5:4 (2分) 5:6(2分)
(3)①④③②(3分)
【解析】
试题分析:(1)等物质的量的NaCl、CaCl2、AlCl3三种溶液中Cl-的量之比为1:2:3,因此产生AgCl沉淀的物质的量之比为1:2:3 。若生成的沉淀的质量相等,则其物质的量也相等,故所需的Cl-的量也相等,因此三种溶液的溶质的物质的量之比为3:2:1 。
(2)设SO2和SO3的质量为m,则其物质的量分别为: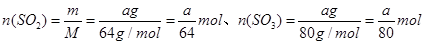 。因此所含分子数之比为:
。因此所含分子数之比为: ;所含O的物质的量之比为:
;所含O的物质的量之比为: 。
。
(3)①所含的原子数为 ;②所含的原子数为
;②所含的原子数为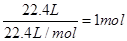 ;③所含的原子数为
;③所含的原子数为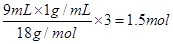 ;④所含的原子数为
;④所含的原子数为 ;因此所含的原子数大小关系为①>④>③>②
;因此所含的原子数大小关系为①>④>③>②
考点:化学计量的相关计算
点评:本题属于基础题,也是高考常考内容。只需掌握常见的计算公式,即可很好的解答此题。


科目:高中化学 来源: 题型:阅读理解
 某学生欲用已知物质的量浓度的盐酸来滴定测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂.请填写下列空白:
某学生欲用已知物质的量浓度的盐酸来滴定测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂.请填写下列空白:| 滴定次数 | 待测氢氧化钠 溶液的体积/mL |
0.1000mol/L盐酸的体积(mL) | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体/mL | ||
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年广东省惠州市实验中学高一上学期期中考试化学试卷(带解析) 题型:填空题
(11分)有关物质的量的计算。
(1)有NaCl、CaCl2、AlCl3三种溶液,若溶质的物质的量相等,分别与足量的硝酸银溶液反应,则生成沉淀的物质的量之比为________________.若生成的沉淀的质量相等,则三种溶液中溶质的物质的量之比为__________。
(2)相同质量的SO2和SO3,所含分子的数目之比为_________;所含O的物质的量之比为________。
(3)下列各物质所含原子数目,按由大到小顺序排列的是
①0.5mol NH3 ②标准状况下22.4L He ③4℃9mL水 ④0.2mol H3PO4
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
(11分)某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,用下图所示装置进行了有关实验:

(1)实验中他们取6.4g铜片和12mL 18mol?L![]() 浓硫酸放在圆底烧瓶中共热,直到反应完毕,最后发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
浓硫酸放在圆底烧瓶中共热,直到反应完毕,最后发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
①请写出铜跟浓硫酸反应的化学方程式:______________________________。
②下列药品中能够用来证明反应结束后烧瓶中确有余酸的是 (填编号)。
A.铁粉 B.BaCl2溶液 C.银粉 D.Na2CO3溶液
③为什么有一定量的余酸但未能使铜片完全溶解,你认为原因是: 。
(2)甲学生设计测定余酸的物质的量浓度的实验方案是测定铜与浓硫酸反应产生SO2的量,再计算余酸的物质的量浓度,他认为测定SO2的量的方法有多种,下列实验方案中不可行的是_____ __(填写字母编号)。
A.将装置A产生的气体缓缓通过预先称量过的盛有碱石灰的干燥管,结束反应后再次称量
B.将产生的气体缓缓通入足量酸性KMnO4溶液,再加入足量BaCl2溶液,过滤、洗涤、干燥、称量沉淀
C.用排水法测定装置A产生气体的体积(标准状况下)
D.用排饱和NaHSO3溶液的方法测出装置A产生气体的体积(标准状况下)
(3)乙学生设计测定余酸的物质的量浓度的实验方案是:测定反应后混合溶液中Cu2+的量。在反应后的溶液中加蒸馏水稀释至100mL,加入足量Na2S溶液,充分反应后过滤,再将沉淀洗涤、干燥、称量。
请写出生成沉淀的离子方程式:
(4)图中C是尾气处理装置,但常常产生倒吸现象,请你设计实验装置,防止倒吸现象的发生,在右图中补充完整:
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com