
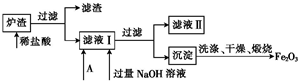


科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| △ |
| A、溶解、过滤、蒸发、洗涤 |
| B、溶解、过滤、洗涤、干燥 |
| C、溶解、蒸发、洗涤、过滤 |
| D、溶解、洗涤、过滤、加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、X、Y、Z的稳定性逐渐减弱 |
| B、A、B、C、D只能形成5种单质 |
| C、X、Y、Z三种化合物的熔、沸点逐渐升高 |
| D、由A、B、C、D四种元素既能组成共价化合物又能组成离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 稀硫酸 |
| △ |
| A、8种 | B、24种 |
| C、16种 | D、32种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
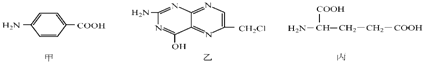
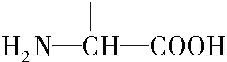 b.在稀硫酸中水解有乙酸生成
b.在稀硫酸中水解有乙酸生成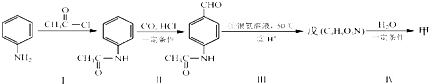
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用小苏打治疗胃酸过多:HCO3-+H+=CO2↑+H2O |
| B、往碳酸钙中滴加稀盐酸:CO32-+2H+=CO2↑+H2O |
| C、往氨水中滴加氯化铝溶液:Al3++3OH-=Al(OH)3 |
| D、氢氧化钡溶液与稀硫酸反应:Ba2++SO42-+H++ OH-=BaSO4↓+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com