
【题目】A、B、C、D、E、F、G均为短周期元素,原子序数依次递增。A元素原子核内无中子,B元素原子最外层电子数是次外层电子数的2倍,D是地壳中含量最多的元素,E是短周期中金属性最强的元素,F与G位置相邻,G是同周期元素中原子半径最小的主族元素。请回答下列问题:
(1)C在元素周期表中的位置为______________,G的原子结构示意图是___________。
(2)D与E按原子个数比1:1形成化合物甲,其电子式为____________________,所含化学键类型为___________________。向甲中滴加足量水时发生反应的化学方程式是___________________________。
(3)E、F、G形成的简单离子,半径由大到小顺序是____________。(用离子符号表示)
(4)用BA4、D2和EDA的水溶液组成燃料电池,电极材料为多孔惰性金属电极。在a极通入BA4气体,b极通入D2气体,则b极是该电池的_____极,负极的电极反应式为_______________________________
【答案】 第二周期ⅤA族 
![]() 离子键和非极性共价键(或离子键和共价键) 2Na2O2+2H2O==4NaOH+O2↑ S2->Cl->Na+ 正 CH4 -8e- + 10OH- = CO32- + 7H2O
离子键和非极性共价键(或离子键和共价键) 2Na2O2+2H2O==4NaOH+O2↑ S2->Cl->Na+ 正 CH4 -8e- + 10OH- = CO32- + 7H2O
【解析】A、B、C、D、E、F、G均为短周期元素,原子序数依次递增.A元素原子核内无中子,则A为氢元素;B元素原子核外最外层电子数是次外层电子数的2倍,则B有2个电子层,最外层有4个电子,则B为碳元素;D元素是地壳中含量最多的元素,则D为氧元素;C原子序数介于碳、氧之间,故C为氮元素;E元素是短周期元素中金属性最强的元素,则E为Na;F与G的位置相邻,G是同周期元素中原子半径最小的元素,可推知F为S元素、G为Cl元素.
(1)C是氮元素,原子有2个电子层,最外层电子数为5,在元素周期表中的位置:第二周期第VA族,G为Cl元素,原子结构示意图是  ,故答案为:第二周期第VA族;
,故答案为:第二周期第VA族; ;
;
(2)D与E按原子个数比1:1形成化合物甲为Na2O2,其电子式为![]() ,所含化学键类型为:离子键、共价键,向过氧化钠中滴加足量水时发生反应的化学方程式是:2Na2O2+2H2O═4NaOH+O2↑,故答案为:
,所含化学键类型为:离子键、共价键,向过氧化钠中滴加足量水时发生反应的化学方程式是:2Na2O2+2H2O═4NaOH+O2↑,故答案为:![]() ;离子键、共价键;2Na2O2+2H2O═4NaOH+O2↑;
;离子键、共价键;2Na2O2+2H2O═4NaOH+O2↑;
(3)电子层结构相同的离子,核电荷数越大离子半径越小,离子电子层越多离子半径越大,故离子半径由大到小的顺序是:S2->Cl->Na+,故答案为:S2->Cl->Na+;
(4)用CH4、O2和NaOH的水溶液组成燃料电池,电极材料为多孔惰性金属电极.在a极通入CH4气体,b极通入O2气体,甲烷发生氧化反应,则a极是该电池的负极,b为正极,氧气在正极获得电子,碱性条件下生成氢氧根离子,正极的电极反应式为:O2+2H2O+4e-═4OH-,负极的反应式为CH4 -8e- + 10OH- = CO32- + 7H2O,故答案为:正;CH4 -8e- + 10OH- = CO32- + 7H2O。


科目:高中化学 来源: 题型:
【题目】工业上常用亚硝酸钠(NaNO2)作媒染剂、漂白剂、钢材缓蚀剂、金属热处理剂。某兴趣小组用下列装置制备NaNO2并探究NO、NO2的某一化学性质(A中加热装置已略去)。

已知:①2NO+Na2O2=2NaNO2;
②NO能被酸性KMnO4氧化成NO3-,MnO4-被还原为Mn2+
请回答下列问题:
(1)装置A三颈烧瓶中发生反应的化学方程式为__________________。
(2)用上图中的装置制备NaNO2,其连接顺序为:a→_____________→h(按气流方向,用小写字母表示),此时活塞K1、K2如何操作_______________________。
(3)E装置发生反应的离子方程式是________________________。
(4)通过查阅资料,NO2或NO可能与溶液中Fe2+发生反应。某同学选择上述装置并按A→C→E顺序连接,E中装入FeSO4溶液,进行如下实验探究。

步骤②操作的目的是__________________;步骤③C瓶中发生的化学方程式为________________;
通过实验可以得出:___________(填“NO2、NO中的一种或两种”)和溶液中Fe2+发生反应使溶液呈深棕色。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一个化学反应,我们不但要关心物质变化,还要研究能量变化和反应快慢。
(1)下面是一个由天然气和水反应制备氢气的反应,其方程式为:CH4(g)+ 2H2O(g) ![]() CO2(g)+4H2(g)该反应过程中能量变化如图所示,则该反应为______反应(填“吸热”或“放热”),
CO2(g)+4H2(g)该反应过程中能量变化如图所示,则该反应为______反应(填“吸热”或“放热”),
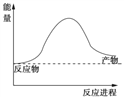
若已知,破坏1mol化学键需要吸收的热量如下表所示:则该反应吸收或放出热量为______kJ (用含a b c d字母的代数式表示)。
化学键 | C—H | O—H | C=O | H—H |
吸收热量(kJ/mol) | a | b | c | d |
(2)一定温度下,将3 molA气体和1mol B气体通入一容积固定为2L的密闭容器中,发生如下反应:3A(g)+B(g) ![]() xC(g),反应1min时测得剩余1.8molA,C的浓度为0.4mol/L,则1min内,B的平均反应速率为________;X为__________。若反应经2min达到平衡,平衡时C的浓度______0.8mol/L(填“大于”,“小于”或“等于”)。若已知达平衡时,该容器内混合气体总压强为p,混合气体起始压强为p0。请用p0、p来表示达平衡时反应物A的转化率为__________。
xC(g),反应1min时测得剩余1.8molA,C的浓度为0.4mol/L,则1min内,B的平均反应速率为________;X为__________。若反应经2min达到平衡,平衡时C的浓度______0.8mol/L(填“大于”,“小于”或“等于”)。若已知达平衡时,该容器内混合气体总压强为p,混合气体起始压强为p0。请用p0、p来表示达平衡时反应物A的转化率为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】北京时间2011年11月3日1时43分,中国自行研制的“神舟八号”飞船与“天宫一号”目标飞行器在距地球343公里的轨道成功对接,为建设空间站迈出关键一步。据悉,所用的动力燃料为N2O4和偏二甲肼[(CH3)2NNH2],下列描述不正确的是
A.偏二甲肼的结构简式可以表达为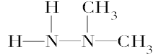
B.偏二甲肼中N元素均为-2价
C. 为偏二甲肼唯一的一种同分异构体
为偏二甲肼唯一的一种同分异构体
D.偏二甲肼与四氧化二氮反应的化学方程式为:(CH3)2NNH2+2N2O4→2CO2+4H2O+3N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】要证明氯乙烷中氯元素的存在可进行如下操作,其中顺序正确的是
①加入AgNO3溶液;②加入NaOH溶液;③加热;④加入蒸馏水;⑤加入HNO3酸化
A.②③⑤① B.④③⑤① C.④①⑤ D.②③①⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表短周期的一部分如表所示.下列有关A、B、C、D、E五种元素的叙述中,正确的是( )
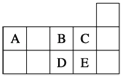
A. D在过量的B中燃烧的主要产物为DB3
B. C的氢化物的水溶液酸性比E的强
C. D与B形成的阴离子可能有DB32﹣、D2B42﹣
D. E单质中由于形成了氢键,所以很容易液化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两个容积相同的容器中,一个盛有C3H8气体,另—个盛有N2O和CO2的混合气体。在同温同压下,两容器内的气体一定具有相同的①分子数②密度③质量④质子数⑤原子数
A. ①②③ B. ①②⑤ C. ③④⑤ D. ①④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实施以减少能源浪费和降低废气排放为基本内容的节能减排政策,是应对全球气候问题、建设资源节约型、环境友好型社会的必然选择。化工行业的发展必须符合国家节能减排的总体要求。试运用所学知识,解决下列问题:
(1)煤化工通常通过研究不同温度下的平衡常数以解决各种实际问题。已知等体积的一氧化碳和水蒸气进入反应器时,会发生如下反应:
CO(g)+H2O(g)![]() H2(g)+CO2(g),该反应的平衡常数随温度的变化如下表所示:
H2(g)+CO2(g),该反应的平衡常数随温度的变化如下表所示:
温度/℃ | 400 | 500 | 800 |
平衡常数K | 9.94 | 9 | 1 |
①若在500℃时进行反应,设CO和H2O的起始浓度均为0.020mol/L,在该条件下,CO的平衡转化率为 。
②800℃时,在固定容积的密闭容器中放入混合物,起始浓度为:c(CO)=0.01mol/L,c(H2O)=0.03mol/L,c(CO2)=0.01mol/L, c(H2)=0.05mol/L ,则反应开始时,H2的消耗速率比生成速率 (填“大”、“小”或“不能确定”)。
(2)2SO2(g)+O2(g)![]() 2SO3(g)反应过程中的能量变化如图所示:又已知1molSO2(g)氧化为1molSO3(g)的ΔH=-99 kJ·mol-1,请回答问题:
2SO3(g)反应过程中的能量变化如图所示:又已知1molSO2(g)氧化为1molSO3(g)的ΔH=-99 kJ·mol-1,请回答问题:
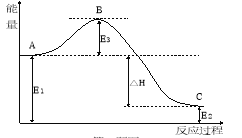
该反应通常用V2O5作催化剂,加V2O5会使图中B点 (填“升高”或“降低” )△H (填“变大”、“变小”或“不变”);
(3)已知某反应的平衡常数表达式为:![]() ,它所对应反应的化学方程式为
,它所对应反应的化学方程式为
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com