
下列各组元素中,都有一种元素的某种性质强于其他元素,表中已选出该元素,并给出六种供选择的理由,请将符合题意的理由编号填入表中.
理由编号:①非金属性最强 ②非金属单质导电性最强 ③最高价氧化物对应的水化物的碱性最强 ④气态氢化物最稳定 ⑤单质沸点最高 ⑥单质与水反应最剧烈

 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
下列各组中的X和Y两元素,一定为同族元素的是 ( )
A.X、Y原子核外电子排布分别为1s2与1s22s2
B.X的M电子层上仅有两个电子,Y的N电子层上仅有两个电子
C.X原子的2p和Y原子的3p都有一个未成对电子,但没有空轨道
D.X、Y最外层都只有一个电子
查看答案和解析>>
科目:高中化学 来源:2013-2014学年北京市东城区高三下学期零模诊断理综化学试卷(解析版) 题型:填空题
A、B、C、D是中学化学常见的四种物质,它们的转化关系如下: A + B = C + D
(1)若A、B、C都是非金属氧化物,且C在空气中易变成A,则A中非氧元素的气态氢化物M的电子
式为 ;分子的稳定性B M(填“>”、“<”或“=”)
(2)若A、D是两种单质,B是黑色有磁性的氧化物,B与盐酸反应生成溶液N,检验N溶液中低价金属阳离子的方法是 。
将D的粉末加入溶液N中,当有28gD完全溶解时,该反应转移的电子是 mol。
(3)若A、B、C、D发生反应:2CO2(g) + 6H2(g) = CH3CH2OH(g) + 3H2O(g),根据下图所示信息,
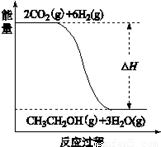
①反应是 反应(填“放热”或“吸热”),判断依据是
②若△H = a KJ/mol,当消耗标况下5.6 L CO2时的反应热 △H = KJ/mol。
③在恒温、恒容的密闭容器中,
下列描述能说明上述反应已达化学平衡状态的是 (填字母序号)。
A.生成1 mol CH3CH2OH的同时,生成3 mol H2O
B.容器中各组份的物质的量浓度不随时间而变化
C.容器中混合气体的密度不随时间而变化
D.容器中气体的分子总数不随时间而变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com