
����Ŀ���ۺ���![]() ��W�������еIJ��ֽṹ����һ����Ҫ�Ĺ��ܸ߷��Ӳ��ϣ��ۺ��������е�һ�֣�ת��·�����£�
��W�������еIJ��ֽṹ����һ����Ҫ�Ĺ��ܸ߷��Ӳ��ϣ��ۺ��������е�һ�֣�ת��·�����£�

��֪����A�й����Ų���ͬһ��̼ԭ���ϡ�
��![]()
��R1CH=CHR2+R3CH=CHR4![]() R1CH=CHR4+R2CH=CHR3(R��ʾ��������ԭ��)��
R1CH=CHR4+R2CH=CHR3(R��ʾ��������ԭ��)��
(1)B����������������__________��
(2)E��������__________��G����H�ķ�Ӧ������__________��
(3)д��D����E�Ļ�ѧ����ʽ��______________________��
(4)X�Ľṹ��ʽ_______________��
(5)E���ڶ���ͬ���칹��,��E������ͬ�������Ҳ��ܷ���������Ӧ��ͬ���칹����__________��(����������ṹ,����E)�����з��Ϻ˴Ź��������з����֮��3��3��2 �Ľṹ��ʽ________________________��
(6)��CH3CH2OHΪԭ��(���Լ���ѡ)�ϳɻ���ϩ,��д���ϳ�����ͼ______��
���𰸡� ȩ������ԭ�� ��ϩ������ ��ȥ��Ӧ CH2=CHCOOH+CH3CH2OH![]() CH2=CHCOOCH2CH3+H2O
CH2=CHCOOCH2CH3+H2O ![]() 7 CH2=C(CH3)COOCH3��CH3COO(CH3)C=CH2 CH3CH2OH
7 CH2=C(CH3)COOCH3��CH3COO(CH3)C=CH2 CH3CH2OH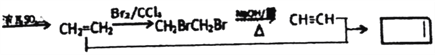
������������֪������̣�A�к��д��ǻ�����ԭ�ӣ������ڲ�̼ͬԭ���ϣ�A��B�������Ĵ�������B��CҲ������������B����ȩ����C�����Ȼ���A��B��C�ķ�Ӧ�в�û�иı���ԭ�ӣ�����B��C��Ҳ������ԭ�ӣ���C��D�ķ�Ӧ�����ɵã�������ȥ��Ӧ�����A�ķ���ʽ���Ƴ�DΪ��CH2=CHCOOH�����Q�Ľṹ��ʽ��D��E�ķ�Ӧ��������֪�ڿɵã�EΪCH2=CHCOOCH2CH3��HΪ![]() ���ٽ��F�ķ���ʽ��F��G�������ɵã�FΪ
���ٽ��F�ķ���ʽ��F��G�������ɵã�FΪ![]() ��GΪ
��GΪ![]() ��
��
��1������������֪��B�к��й�����Ϊȩ������ԭ�ӡ�
��2��EΪCH2=CHCOOCH2CH3����CH2=CHCOOH(��ϩ��)���Ҵ���Ӧ���ɵ������������DZ�ϩ��������GΪ![]() ��HΪ
��HΪ![]() ������G������ȥ��Ӧ���ɵ�H��
������G������ȥ��Ӧ���ɵ�H��
��3��DΪCH2=CHCOOH��EΪCH2=CHCOOCH2CH3����Ϸ�Ӧ�����ɵã�D(CH2=CHCOOH)���Ҵ�����������Ӧ����EΪ(CH2=CHCOOCH2CH3)����D����E�Ļ�ѧ����ʽ����CH2=CHCOOH+CH3CH2OH![]() CH2=CHCOOCH2CH3+H2O��
CH2=CHCOOCH2CH3+H2O��
��4���ɾۺ���X��![]() (W�������еIJ��ֽṹ)��һ�֣������֪�ۼ�������Q��X�ɵã�XΪ
(W�������еIJ��ֽṹ)��һ�֣������֪�ۼ�������Q��X�ɵã�XΪ![]() ��
��
��5��EΪCH2=CHCOOCH2CH3����E������ͬ�������Ҳ��ܷ���������Ӧ��ͬ���칹������CH3CH=CHCOOCH3��CH2=CHCH2COOCH3��CH2=C(CH3)COOCH3��CH3COOCH2=CHCH3��CH3COOCH2CH=CH2��CH3COO(CH3)C=CH2��CH3CH2COOCH=CH2��7�� (����������ṹ������E)�����з��Ϻ˴Ź��������з����֮��3:3:2�Ľṹ��ʽΪ��CH2=C(CH3)COOCH3��CH3COO(CH3)C=CH2��
��6������֪�ڵõ���������CH3CH2OHΪԭ��(���Լ���ѡ)�ϳɻ���ϩ����Ҫ��ϩ����Ȳ�����ɻ���Ӧ���Ҵ���ȥ��Ӧ�ɵõ���ϩ������ϩ�ɽ�һ���õ���Ȳ���ʺϳ�����Ϊ��![]() ��
��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������绯��ʴ�ص���
A. ��ͭ��ͭп�Ͻ�������ͭ��ײ���ͭ��
B. ����������о�������Ǵ�������������
C. ������������ͭ��������ڽӴ�����������
D. ���ʽ��ƾ��ú����䰵
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ɽ�����������̼-̼ż����Ӧ�ǽ������л��ϳɵ��о��ȵ�֮һ,��:
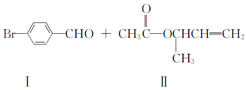
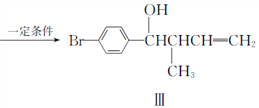
��1�����������ķ���ʽΪ_____________���䱽���ϵ�һ�ȴ�����______________�֡�
��2���������������������ŵ�������__________________��
��3�����ڷ��㻯�������___________________(�����)��
��4�������������е��ǻ���Brȡ������д����ȡ�������ܷ��������з�Ӧ����_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�������̻�(��Ҫ��PbO��As2S3��In2O2��In2S3��) Ϊԭ�ϻ���ϡɢ������(In)������ϡȱ��Դ����ҪӦ������������Ϳ�㡢ӫ����ϡ��л��ϳɵȣ�����������������������̼�������������:
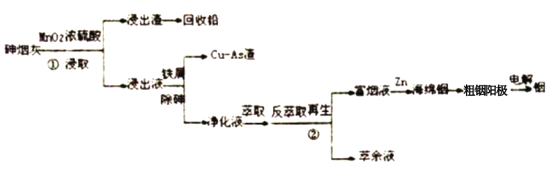
���̻ҵ��������������������
��Ŀ | Һ�̱� | ʼ�����(g��L-l) | �������(g��L-l) | �¶�(��) | ʱ��(h) | �̷ۼ�����(%) |
һ�ν��� | 3~7��1 | 90-120 | 30-80 | >95 | >4 | 3~7 |
����� | 3~7��1 | 150-180 | 120-150 | >95 | >4 | 10-15 |
��1�� ������Ҫ��ν��л����ķ��룬���в����ٵķ��뷽���ֱ�Ϊ_________���ڵķ��뷽����ʵ������ʹ�õ���Ҫ����Ϊ_________ ��
��2�������й�����˵������ȷ����_________��
A.���ν�ȡʱ�¶�Խ�ߣ�����ʱ��Խ������ҵЧ��Խ��
B.��ȡʱ�������˵�Һ�̱ȣ��ȿ�Ϊ�²���ȡ�ṩ���ʵ���ȣ����ܵõ��ϸ�Ũ�ȵ�In3+��Һ
C.����Һͨ����ȡ������ȡ�������ȹ��̿ɸ����õ���Ũ��In3+��Һ��ʹ��ȡ��ѭ������
D.������ʱ������ɷְ���п��ͭ�����Ƚ���
��3����ȡ����Һ���ñ�ȡ������H2A2��ʾ��ʹIn3+�����л��࣬��ط�Ӧ�ɱ�ʾΪ: In3++3H2A2![]() In (HA2)3+3H+�� ����ȡ�����Լ�Ӧѡ��_______(ѡ ��:�� ϡ����������NaOH��Һ��)
In (HA2)3+3H+�� ����ȡ�����Լ�Ӧѡ��_______(ѡ ��:�� ϡ����������NaOH��Һ��)
��4�����̻��е�As2S3������ϡ���ᣬ������MnO2����ܽ⣬��ת��ΪAsO43-��ͬʱ������������ζ���塣�÷�Ӧ�Ļ�ѧ����ʽΪ______________��
��5����⾫������ʱ��������Ӧѡ��________�����ŵ��IJ��Ͻ��У����Һ��c(In3+)����________(��:��������������С������������)��
��6����ҵ�ϳ�����ITO�вķ��ϻ������������Һ����Ҫ��Sn4+���ʣ����ӿɲ��ü���Na2S��Һ�ķ�����ҪʹSn4+������ȫ��c(Sn4+)����10-5mol/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ҫ����500 mL 0.5 mol��L��1����������Һ�����ⶨʵ����������������Һ��Ũ��Ϊ0.45 mol��L��1�����ܵ�ԭ����(����)
A. ת��ʱ��Һû����ȴ������ B. ����ƿû�к��
C. �����������ƹ���ʱ����ŷ��� D. ����ʱ���Ӷ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ի�ѧ��Ӧ�����ʺ��ȵ�������ȷ���ǣ� ��
A.����ijһ��Ӧ�������һ���ܹ��ӿ�÷�Ӧ������
B.��ѧ��Ӧ�����Dz��ɸı��
C.��ѧ��Ӧ���е�ʱ��Խ���÷�Ӧ����Խ��
D.��ѧ��Ӧ�ﵽ��ʱ�����淴Ӧ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���й�������![]() �����������У�����֤������������ʵ��ǣ� ��
�����������У�����֤������������ʵ��ǣ� ��
A. ![]() ��������Һ��pHԼΪ4
��������Һ��pHԼΪ4
B. �����£�![]() a��HCNϡ��100����������Һ
a��HCNϡ��100����������Һ![]() a
a![]()
C. KCN��Һ�ʼ���
D. ![]() ǡ����
ǡ����![]() ��Һ��ȫ��Ӧ
��Һ��ȫ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ڷ�����ᴿ���ʵķ����У����ˡ������ᾧ��������ȡ����Һ��ϴ������������������װ�õ���Ų����ϲ������ƣ�


��1������Na2CO3��Һ��CCl4��ѡ_____����������Ϊ________��
��2����CCl4��ȡ��ˮ�еĵ⣬ѡ______����������Ϊ________��
��3��������������Һ����O2�л��е�����Cl2��ѡ_______����������Ϊ________��
��4����ȥ����ʯ��ˮ��������CaCO3����ѡ______����������Ϊ__________��
��5����ȡ����ˮ��ѡ________����������Ϊ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ҫ��ϡȱս����Դ���㷺Ӧ�����ڶ�����������������������ҹ�ս���մ�������ij���п�����õ���ȡ�༼��·��Ϊ����Ʒλ�ྫ��-�������������Ȼ�ԭ-��ջӷ�������-�ӷ������Ʒλ��ԭ�ྫ��-������Ԥ����-���������ᴿ-�ߴ����Ȼ���-�ߴ��������ࡣ

��1�������ڱ��н�����ǽ����ķֽ紦�������ҵ��뵼����ϣ���Si�� �ȣ��뵼���������������ǿ�ʼ�� ��������չ����������ͬ��� ������Ԫ��������_______�����ţ���
a��Ge Si Ge
b��Ge Ge Si
c��C Si Ge
��2������ƽ�����������Ȼ�ԭ��Ӧ�Ļ�ѧ����ʽ����������ע����Ӧ������
___NaH2PO2��H2O+GeO2 ![]() ___Na4P2O7+___H2O+___GeO��+___H3PO4��_____________
___Na4P2O7+___H2O+___GeO��+___H3PO4��_____________
��3����Ʒλ��ԭ�ྫ�������Ԥ�������̵IJ����������ƣ���д���ù��̵Ļ�ѧ��Ӧ����ʽ��____________________________________________
��4���ߴ��������ຬ�����õ���صζ������з�������ȡ3.600g�ߴ�����������Ʒ���������������ڵ�¯�����������������Ƽ��Ȼ�ԭ��Ȼ���Ե���Ϊָʾ�����õ���ر���Һ��0.6000mol/L���ζ������ĵĵ�������Ϊ19.00mL��[20�����£����������Ʋ��ᱻ����غ͵�����]
�ٵζ��յ��������_____________________________��
�ڴ���Ʒ�ж������ຬ����_________����������λ��Ч���֣�
��5����������ԭGeO2���Ƶý����ࡣ�䷴Ӧ���£�
GeO2+ H2= GeO+ H2O ��
GeO+ H2= Ge+ H2O ��
GeO2+ 2H2= Ge+ 2H2O ��
��Ӧʽ����H=+13750 kJ/mol ����S=+15600J/(K��mol������ԭ��Ӧ���¶�һ�������_________����Χ�ڡ�[��֪GeO��700����������T(K)=t(��)+273]
��6�����������е��ܽ��ٶ�������Ũ�ȡ������ٶȡ��¶ȵ�����Ӱ�졣��ͼ�����ܽ��ٶ���һ���ֵ�������Ũ��С�ڴ�ֵʱ����Ũ�������ܽ��ٶ����ӣ���֮���ͣ�������������Ũ�ȸ�ʱ_________�Ӿ����¡�
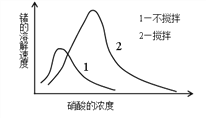
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com