
����Ŀ����1x105Pa��298 Kʱ����1 mol��̬AB���ӷ������̬Aԭ�Ӻ�Bԭ������Ҫ��������ΪA-B���ۼ��ļ���( kJ/mol)��������һЩ���ۼ��ļ��ܣ���֪����������3���ȼ۵ĵ���ۼ�����
���ۼ� | H-H | N��N | N-H |
���ܣ�kJ/mol�� | 436 | 945 | 391 |
��1�������ϱ��е������жϹ�ҵ�ϳɰ��ķ�Ӧ��N2(g)+3H2(g)![]() 2NH3(g)��____��������������������������Ӧ��
2NH3(g)��____��������������������������Ӧ��
��2����298 Kʱ��ȡ1mol������3mol��������һ�ܱ������У����ڴ�������������ǡ����ȫ��Ӧ�������Ϸų������յ�����ΪQ1��Q1����ֵ��____��
��3��ʵ�������У��ų������յ�����ΪQ2������ѡ����ȷ����____����ѡ����ţ���
A��Q1>Q2 B��Q1<Q2 C��Q1=Q2
��������ѡ���ԭ����________��
���𰸡����� 93kJ A �÷�ӦΪ���淴Ӧ�����ܱ������з�Ӧ�ﵽƽ��ʱ��1molN2��3molH2������ȫ��Ӧ����2molNH3������ų�������С��93kJ
��������
(1)���ݼ�����ⷴӦ�ȣ�
(2)(3)���淴Ӧ�뷴Ӧ�ȵĹ�ϵ��
(1)�Ͽ���ѧ����Ҫ������������Ͽ�1molN��N��3molH-H��������945kJ+3��436kJ=2253kJ���������γ�6molN��H�����ͷ�6��391kJ=2346kJ���������ͷŵ����������յ������࣬��÷�ӦΪ���ȷ�Ӧ��
(2)1molN2��3molH2��������2molNH3�����շ���ʽ�ͷ�2346kJ-2253kJ=93kJ������Q1����ֵΪ93kJ��
(3)N2��H2��ӦΪ���淴Ӧ�����ܱ������з�Ӧ�ﵽƽ��ʱ��1molN2��3molH2����������2molNH3�������ͷŵ�������93kJ�٣�ѡA��


 Сѧ�̲���ȫ���ϵ�д�
Сѧ�̲���ȫ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������ᣬ�䱾����NO3���������ԣ�ij����ʵ��С������������й�NO3�������Ե�̽����ʵ�����ͨ�������ɣ���
ʵ��װ�� | ��� | ��ҺX | ʵ������ |
| ʵ��� | 6 mol��L-1ϡ���� | ������ָ������ƫת��ͭƬ���������ɫ���壬��Һ���Ϸ���Ϊ����ɫ�� |
ʵ��� | 15 mol��L-1Ũ���� | ������ָ��������ƫת���ܿ���ƫ����ߣ���Ƭ��ͭƬ�����������ɫ���壬��Һ��Ϊ��ɫ�� |
��1��ʵ����У���Ƭ��_____�����������������Һ���Ϸ���������ɫ����Ļ�ѧ����ʽ��_________��
��2��ʵ����е�����ָ����ƫ���ұߺ�ƫ�������ԭ����____________________��
�������ϣ����ý�����1 mol��L-1ϡ���ᷴӦ��H2��NH4+���ɣ�NH4+���ɵ�ԭ���Dz���H2�Ĺ�����NO3������ԭ��
��3������ͼװ�ý���ʵ�����ҺXΪ1 mol��L-1ϡ������Һ���۲쵽������ָ���� ��ƫת��
�ٷ�Ӧ�����Һ�к�NH4+��ʵ���Ҽ���NH4+�ķ�����______________________________��
������NH4+�ĵ缫��Ӧʽ��_____________________________________________��
��4����һ��̽������������NO3���������ԣ�����ʵ�����

�ٹ۲쵽A����NH3���ɣ�B������������A��B������ͬ����Ľ�����_______________��
��A������NH3�����ӷ���ʽ��_______________________________��
��5�������ۼ��뵽NaNO3��Һ�������������ʵ���͢�˵������_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ѽ���ȡ�����ķ�ӦΪ2H2S(g)![]() 2H2(g)+S2(g)��������ܱ������г���һ������H2S���壬�����ϵ�������ƽ��������¶ȵĹ�ϵ��ͼ��ʾ������˵����ȷ����
2H2(g)+S2(g)��������ܱ������г���һ������H2S���壬�����ϵ�������ƽ��������¶ȵĹ�ϵ��ͼ��ʾ������˵����ȷ����

A. �÷�Ӧƽ�ⳣ�����¶����߶�����
B. M��ʱ������������ѹǿ��N�Ĵ�
C. M��ʱ��H2S��ƽ��ת����Ϊ50%
D. ά��M���¶Ȳ��䣬���������ٳ���0.2molH2S��0.2molH2��0.1molS2(g)����v(��) = v(��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ����٤��������ֵ������������ȷ���ǣ�������
A. 1L1.0mo1L-1��NaAlO2ˮ��Һ�к��е���ԭ����Ϊ2NA
B. ��״���£�11.2LNO��11.2LO2��Ϻ�����������Ϊ0.75NA
C. Na2O��Na2O2���������ʵ���Ϊ1mol�����к��е�����������ΪNA
D. �����£���9g��ƬͶ��0.5L 18.4molL-1��H2SO4�У�ת�Ƶĵ�����ΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����յ�һ�������ɴ�С��˳�����д�����ǣ� ��
A. Be��Mg��Ca B. Na��Mg��Al C. He��Ne��Ar D. Li��Na��K
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ�п��ܺ���OH����CO32����AlO2-��SiO32-��SO42-��Na����Fe3����Mg2����Al3�������ӡ��������Һ�м���һ�����ʵ���Ũ�ȵ�������Һʱ���������ɳ��������ʵ�����������Һ������仯��ͼ����ͼ��ʾ������˵����ȷ������ ��

A. ԭ��Һ��һ�����е���������OH����SiO32-��AlO2-��CO32��
B. ��Ӧ����γɵ���Һ�е�����ΪNaCl
C. ԭ��Һ��һ������Na2SO4
D. ԭ��Һ��CO32����AlO2-�����ʵ���֮��Ϊ1��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������[KAl(SO4)2��12H2O]��һ���Σ�����ֽ�ȷ���Ӧ�ù㷺��ij��ȤС�����10.0g��������(��90%��Al��������������Fe��Mg�����ʣ��Ʊ�������ʵ�鷽�����£�
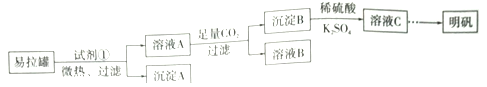
��1���Լ���Ӧѡ��_____________(����ţ���
a.���� b.H2SO4��Һ c.�Ȼ�����Һ d.NaOH��Һ
��2���������ܽ��������Ҫ��Ӧ�Ļ�ѧ����ʽΪ____________________��
��3����ҺB�����ʵ���Ҫ�ɷ�Ϊ____________________ (�ѧʽ)��
��4������ҺC�еõ�������ʵ���������Ϊ����Ũ����__________(��������ƣ������ˡ�ϴ�ӡ��������ͼ��ʾ�����������е�һ��������_____________��

��5����С����ʵ�����֮�õ�118.5 g�������������Ļ�����Ϊ_____________������֪��������Ħ������Ϊ474g��mol-1)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��MnO2+4HCl(Ũ)![]() MnCl2+Cl2��+2H2O��Ӧ������˵����ȷ���ǣ� ��
MnCl2+Cl2��+2H2O��Ӧ������˵����ȷ���ǣ� ��
A. ÿ����1molMnO2����Cl2�����Ϊ22.4L
B. �������뻹ԭ�������ʵ���֮��Ϊ1:4
C. �����ԣ�MnO2>Cl2
D. ��Ӧ��ÿ����1molCl2ʱ��ת�Ƶ��ӵ����ʵ���Ϊ4mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��ȷ����
A. ������ˮ��Ӧ��Cl2+H2O ![]() Cl-+ClO��+2H+
Cl-+ClO��+2H+
B. �������Һ������������Һ��Ӧ��Ba2++SO42��=BaSO4��
C. ��������������Һ�ڿ����б�������4Fe2����O2��4H����4Fe3����2H2O
D. ̼��������Һ�����ij���ʯ��ˮ��ϣ�2HCO3��+Ca2++2OH��=CaCO3��+CO32��+2H2O
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com