
下列说法不正确的是
A.在纯水中加入能水解的盐一定促进水的电离
B.NH4F水溶液中含有HF,因此NH4F溶液不能存放于玻璃试剂瓶中
C.加热CH3COONa溶液,溶液中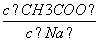 的值将减小
的值将减小
D.常温下醋酸分子不可能存在于pH>7的碱性溶液中
科目:高中化学 来源: 题型:
(1)中和热的测定是高中化学的定量实验之一.50 mL0.50 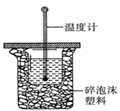 mol/L 盐酸与50 mL
mol/L 盐酸与50 mL
0.55 mol/L NaOH 溶液在如图所示的装置中进行中和反应。
通过测定反应过程中所放出的热量可计算中和热。从实验
装置上看,图中尚缺少的一种仪器是 。大烧杯上如不
盖硬纸板,求得的中和热数值将会
(填“偏大”、“偏小”或“无影响”)。
(2)氧化剂H2O2在反应时不产生污染物,被称为绿色氧化剂,因而受到人们越
越多的关注。
Ⅰ.某实验小组以H2O2分解为例,探究浓度、催化剂、溶液酸碱性对反应速率的
影响。在常温下按照下表所示的方案完成实验。
| 实验编号 | 反应物 | 催化剂 |
| ① | 10 mL 2% H2O2溶液 | 无 |
| ② | 10 mL 5% H2O2溶液 | 无 |
| ③ | 10 mL 5% H2O2溶液 | 1 mL 0.1 mol·L-1FeCl3溶液 |
| ④ | 10 mL 5% H2O2溶液+少量HCl溶液 | 1 mL 0.1 mol·L-1FeCl3溶液 |
| ⑤ | 10 mL 5% H2O2溶液+少量NaOH溶液 | 1 mL 0.1 mol·L-1FeCl3溶液 |
(1)实验①和②的目的是________。
同学们进行实验时没有观察到明显现象而无法得出结论。资料显示,通常条
件下H2O2稳定,不易分解。为了达到实验目的,你对原实验方案的改进方法
 是 ________(填一种即可)。
是 ________(填一种即可)。
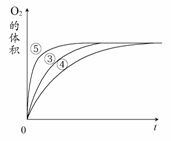
实验③④⑤中,测得生成氧气的体积随时间变化
的关系右图所示。
分析该图能够得出的实验结论是________。
Ⅱ.资料显示,某些金属离子对H2O2的分解起催化作用。为比较Fe3+和Cu2+对H2O2
分解的催化效果,该实验小组的同学设计了如图所示的实验装置进行实验。
某同学通过测定O2的体积比较H2O2的分解速率快慢,实验时可以通过测量
________ 或 ________比较;
(2)0.1g MnO2粉末加入50 mL H2O2溶液中,在标准状况下放出气体的体积和时
间的关系如图所示。解释反应速率变化的原因:________,计算H2O2的初始物
质的量浓度为________。(保留两位有效数字,在标准状况下测定)
Ⅲ.(1)为了加深对影响反应速率因素的认识,老师让甲同学完成下列实验:
在Ⅱ中的实验装置的锥形瓶内盛6.5g锌粒(颗粒大小基本相同),通过分液
漏斗加入40 mL 2.5 mol/L的硫酸,10s时收集产生的H2体积为50 mL
(若折合成标准状况下的H2体积为44.8mL),用锌粒表示10s内该反应的速
率为______g/s;
根据化学反应速率与化学平衡理论,联系化工生产实际,你认为下列说法
不正确的是________(填序号)。
A.化学反应速率理论可以指导怎样在一定时间内快出产品
B.勒夏特列原理可以指导怎样使有限原料多出产品
C.催化剂的使用是提高原料转化率的有效办法
D.正确利用化学反应速率和化学反应限度都可以提高化工生产的综合经济效益
查看答案和解析>>
科目:高中化学 来源: 题型:
糖类、脂肪和蛋白质是维持人体生命活动所必需的三大营养物质。以下叙述正确的是
A.植物油不能使溴水褪
B.淀粉水解的最终产物是葡萄糖
C.葡萄糖能发生氧化反应和水解反应
D.蛋白质溶液遇硫酸铜后产生的沉淀能重新溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)淀粉的化学式是 ;玻璃、陶瓷、水泥一定含 元素。造成赤潮的主要元素
是 ;油脂在体内水解后的产物是 和高级脂肪酸。
(2)常见的塑料有两类,一类是 塑料,如聚乙烯,一类是 塑料,如酚醛树脂等。
硫化后的橡胶适合制造汽车轮胎,加入 可增强轮胎的耐磨性。
(3)在“棉花、尼龙、黏胶纤维、蚕丝”这四中纤维中,属于天然纤维的是 ;属于
人造纤维的是 ;属于合成纤维的是 。
(4)药品标签上应贴有 “OTC”或“R”符号,①“OTC”它表示 ,②“R”表示 ,
氢氧化铝和碳酸氢钠都可用作抗胃酸药。写出:
③氢氧化铝与胃酸作用的离子方程式: ;
④碳酸氢钠与胃酸作用的化学方程式: 。
(5)一个体重50kg的健康人,体内约含有2g铁,这2g铁在人体内不是以单质的形式存在,而
是以Fe2+ 和Fe3+的形式存在。正二价铁离子易被吸收,给贫血者补充铁时,应给予含Fe2+
的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的Fe3+还原成Fe2+,有利于人体吸收。
①往KMnO4溶液中滴入维生素C溶液,KMnO4溶液褪色说明维生素C具有 性,
②人体长期缺乏维生素C会引起 病,
③市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸的作用下
转化成亚铁盐。此反应的离子方程式为
(6)我国城市为了减少燃煤造成的大气污染,对民用燃料的煤作了多方面的改进。
①绿色能源是人类的理想能源不会造成环境污染,下列能源不属于绿色能源的是
A.氢能源 B.太阳能 C.风能 D.石油
②为了除去煤中的含硫化合物,采用FeCl3脱硫,即用FeCl3溶液浸洗煤粉,发生如下反
应:FeS2+14FeCl3+8H2O===2FeSO4+13FeCl2+16HCl 该反应中的氧化剂是 ;
为了充分利用Fe2+并减少酸(HCl)污染,本方法中可利用工业废铁屑和氯气让废液重新
利用生成FeCl3。请写出这一过程中有关的离子方程式:
、 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式正确的是:
A、等体积、等浓度的Ba(OH)2溶液与KAl(SO4)2溶液混合:
3Ba2++6OH-+2 Al3++3SO42-===3BaSO4↓+2Al(OH)3↓
B、向NaAlO2溶液中通入过量CO2: 2AlO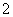 +CO2+3H2O===2Al(OH)3↓+CO
+CO2+3H2O===2Al(OH)3↓+CO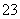
C、Fe3O4与稀硝酸反应的离子方程式为: Fe3O4+8H+===Fe2++2Fe3++4H2O
D、向NaOH溶液中加入金属铝:Al+2OH- === AlO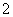 +2H2O
+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
已知常温下,AgBr的Ksp=4.9×10-13 mol2·L-2、AgI的Ksp=8.3×10-17 mol2·L-2 下列说法正确的是:
A、在常温下AgI水溶液中,Ag+和I-浓度的乘积是一个常数
B在常温下,在任何含AgI固体的溶液中,c(Ag+)=c(I-)且Ag+与I-浓度的乘积等于8.3×10-17 mol2·L-2
C常温下,将1mL 1.0×10-2 mol/L的KI与AgNO3溶液等体积混合,则生成AgI沉淀所需AgNO3溶液的最小浓度为3.32×10-14 mol/L
D、向AgI饱和溶液中加入AgBr固体,c(I-)不变,Ksp值不变
查看答案和解析>>
科目:高中化学 来源: 题型:
下列推断正确的是
A.SO2和CO2都是酸性氧化物,都能与NaOH溶液反应
B.Na2O和Na2O2组成元素相同,与CO2反应产物也完全相同
C.NO和NO2的密度都比空气大,都可以用向上排空气法收集
D.C3H8和CH3CH2OH相对分子质量相近,二者沸点也相近
查看答案和解析>>
科目:高中化学 来源: 题型:
在36 g 碳不完全燃烧所得气体中,CO占 体积,CO2占
体积,CO2占 体积,且
体积,且
C(s) + 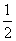 O2(g) = CO(g) △H = -110.5 kJ/mol
O2(g) = CO(g) △H = -110.5 kJ/mol
CO(g) + 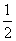 O2(g) = CO2(g) △H = -283 kJ/mol
O2(g) = CO2(g) △H = -283 kJ/mol
与这些碳完全燃烧相比,损失的热量是
A.172.5 kJ B. 1149 kJ C.283kJ D. 517.5 kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com