
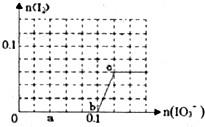
 ��֪����ԭ��HSO3-��I-��������IO3-��I2���ں�0.3mol NaHSO3����Һ����μ���KIO3��Һ������KIO3������I2�����ʵ����Ĺ�ϵ������ͼ��ʾ������˵������ȷ���ǣ�������
��֪����ԭ��HSO3-��I-��������IO3-��I2���ں�0.3mol NaHSO3����Һ����μ���KIO3��Һ������KIO3������I2�����ʵ����Ĺ�ϵ������ͼ��ʾ������˵������ȷ���ǣ�������| A��0��b��ķ�Ӧ�����������ӷ���ʽ��ʾ��3HSO3-+IO3-�T3SO42-+I-+3H+ | B��a��ʱ����NaHSO3�����ʵ���Ϊ0.12mol | C������Һ��I-��I2�����ʵ���֮��Ϊ5��2ʱ�������KIO3Ϊ0.18mol | D��b��ʱ�Ļ�ԭ���������KI��NaI��b��c��Ļ�ԭ������I2 |
| 0.04mol |
| 1 |
| 1 |
| 3 |
| 5 |
| 3 |
| 5 |
| 3 |
| 5 |
| 3 |
| 1 |
| 3 |


 �ο�������ϵ�д�
�ο�������ϵ�д� ������ѧ��ʱ��ҵϵ�д�
������ѧ��ʱ��ҵϵ�д� ���������ʱ��ѵϵ�д�
���������ʱ��ѵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ���㽭ʡ�����н���������֯������ѧ������������ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪����ԭ��HSO3¯>I¯��������IO3¯> I2 ���ں�3 mol NaHSO3����Һ����μ���KIO3��Һ������KIO3������I2�����ʵ����Ĺ�ϵ��������ͼ��ʾ������˵������ȷ����
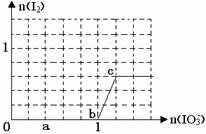
A��0--b ��3HSO3�� + IO3�� �� 3SO4���� + I�� + 3H��
B��a��ʱ����NaHSO3�����ʵ���Ϊ1��2 mol
C��b��ʱ�Ļ�ԭ���������KI��NaI��b~c��Ļ�ԭ������I2
D������Һ��I¯��I2�����ʵ���֮��Ϊ5��2ʱ�������KIO3Ϊ1��8mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ�꽭��ʡ������ѧ�����п��Ի�ѧ�Ծ� ���ͣ�ѡ����
��֪����ԭ��HSO3¯>I¯��������IO3¯> I2 .�ں�3 mol NaHSO3����Һ����μ���KIO3��Һ.����KIO3������I2�����ʵ����Ĺ�ϵ��������ͼ��ʾ.����˵����ȷ���ǣ� ��
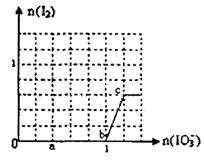
A����Ӧ�����е����������ΪSO3
B��a��ʱʣ��NaHSO3�����ʵ���Ϊ1.8 mol
C��c��ʱ�Ļ�ԭ���������KI��NaI
D������Һ��I¯��I2�����ʵ���֮��Ϊ1:1ʱ�������KIO3Ϊ1.2mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010-2011ѧ���Ϻ��и�����ѧ�����п��Ի�ѧ�Ծ� ���ͣ�ѡ����
��֪����ԭ��HSO3¯>I¯��������IO3¯> I2 ���ں�3 mol NaHSO3����Һ����μ���KIO3��Һ������KIO3������I2�����ʵ����Ĺ�ϵ��������ͼ��ʾ��
����˵����ȷ����

A����Ӧ�����е����������ΪSO3
B��a��ʱʣ��NaHSO3�����ʵ���Ϊ1.2 mol
C��b��ʱ�Ļ�ԭ���������KI��NaI
D������Һ��I¯��I2�����ʵ���֮��Ϊ1:1ʱ�������KIO3Ϊ9/8mol
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com