
| A、①③ | B、③④⑤ | C、②③ | D、全部 |


 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案科目:高中化学 来源: 题型:
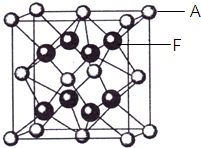 三氟化氮(NF3)是一种无色、无味、无毒且不可燃的气体,在半导体加工、太阳能电池制造和液晶显示器制造中得到广泛应用.它可在铜的催化作用下由F2和过量的NH3反应得到,该反应另一种产物为盐.
三氟化氮(NF3)是一种无色、无味、无毒且不可燃的气体,在半导体加工、太阳能电池制造和液晶显示器制造中得到广泛应用.它可在铜的催化作用下由F2和过量的NH3反应得到,该反应另一种产物为盐.查看答案和解析>>
科目:高中化学 来源: 题型:
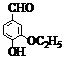 )是食品添加剂的增香原料,香味比香草醛更浓郁.
)是食品添加剂的增香原料,香味比香草醛更浓郁.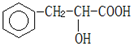 )在浓硫酸条件下加热能发生消去反应生成有机物B.写出由A生成B的化学方程式:
)在浓硫酸条件下加热能发生消去反应生成有机物B.写出由A生成B的化学方程式: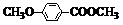 )是一种医药中间体.请设计合理方案用茴香醛(
)是一种医药中间体.请设计合理方案用茴香醛(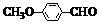 )合成D(其他原料自选,用反应流程图表示,并注明必要的反应条件)
)合成D(其他原料自选,用反应流程图表示,并注明必要的反应条件)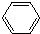
| H2△ |
| 催化剂 |
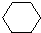
| Br2 |
| 光照 |
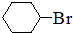
查看答案和解析>>
科目:高中化学 来源: 题型:
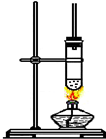 1-丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度为115~125℃,反 应装置如图.下列对该实验的描述错误的是( )
1-丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度为115~125℃,反 应装置如图.下列对该实验的描述错误的是( )| A、不能用水浴加热 |
| B、长玻璃管起冷凝回流作用 |
| C、提纯乙酸丁酯需要经过水、氢氧化钠溶液洗涤 |
| D、浓硫酸的作用是催化剂和吸水剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
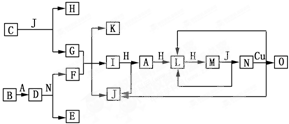
查看答案和解析>>
科目:高中化学 来源: 题型:
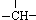 ,其余为-NH2,则-NH2的数目可能是( )
,其余为-NH2,则-NH2的数目可能是( )| A、2n+3-m |
| B、a+2-m |
| C、n+m+a |
| D、a+2n+2-m |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com