
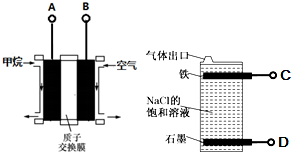
| A. | 燃料电池的A极连接电解池的C极 | |
| B. | A电极的电极反应式为:CH4-8e-+2H2O=CO2+8H+ | |
| C. | 燃料电池工作时H+移向左边 | |
| D. | 电解池总反应式为NaCl+H2O$\frac{\underline{\;电解\;}}{\;}$NaClO+H2↑ |
分析 利用甲烷燃料电池电解饱和食盐水制备漂白液的原理:在阴极上产生氢气,在阳极上产生氯气和氢氧化钠,氯气和氢氧化钠反应生成氯化钠和次氯酸钠和水,所以D处产生的是氯气,C处产生的是氢气,根据原本电池的工作原理以及电极反应式来回答判断.
解答 解:利用甲烷燃料电池电解饱和食盐水制备漂白液的原理:在阴极C上产生氢气,在阳极上产生氯气和氢氧化钠,氯气和氢氧化钠反应生成氯化钠和次氯酸钠和水,所以D处产生的是氯气,C处产生的是氢气.
A、燃料电池中通入燃料甲烷的电极A是负极,C是阴极,A极连接电解池的C极,故A正确;
B、A电极是负极,燃料发生失电子的氧化反应,其电极反应式为:CH4-8e-+2H2O=CO2+8H+,故B正确;
C、燃料电池中阳离子移向正极,即移向右边,故C错误;
D、电解饱和食盐水制备漂白液次氯酸钠,电解池总反应式为NaCl+H2O$\frac{\underline{\;电解\;}}{\;}$NaClO+H2↑,故D正确.
故选C.
点评 本题考查了原电池和电解池原理及物质的量的有关计算,注意知识的归纳和梳理是解题的关键,难度中等.


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:解答题
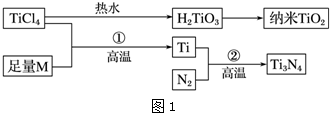
| I1 | I2 | I3 | I4 | I5 | |
| 电离能/kJ•mol-1 | 738 | 1451 | 7733 | 10540 | 13630 |
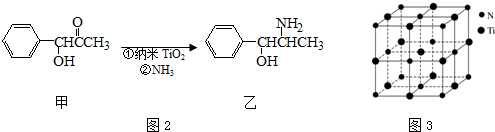
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ•mol-1 | 786 | 715 | 3401 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| A | 完全燃烧的产物中n(CO2):n(H2O)=2:1 28<Mr(A)<60 不能使溴的四氯化碳溶液褪色 一氯代物只有1种结构 |
| B | 饱和链烃,通常情况下呈气态 二溴代物有3种 |
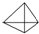 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化合物:干冰、冰水共存物、烧碱、小苏打 | |
| B. | 非电解质:乙醇、四氯化碳、氯气、葡萄糖 | |
| C. | 同素异形体:活性炭、C60、石墨烯、金刚石 | |
| D. | 混合物:铝热剂、纯净矿泉水、分析纯盐酸、漂白粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
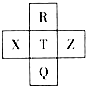 元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示,其中R单质在暗处与H2剧烈化合并发生爆炸.则下列判断正确的是( )
元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示,其中R单质在暗处与H2剧烈化合并发生爆炸.则下列判断正确的是( )| A. | 非金属性:Z<T<X | B. | R与Q的电子数相差26 | ||
| C. | 气态氢化物稳定性:R<T<Q | D. | 最高价氧化物的水化物的酸性:R>Q |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com