
下列关于晶体的说法中,不正确的是( )
①晶胞是晶体结构的基本单元
②分子晶体若是密堆积方式,其配位数都是12
③含有离子的晶体一定是离子晶体
④共价键的强弱决定分子晶体熔沸点的高低
⑤MgO远比NaCl的晶格能大
⑥含有共价键的晶体一定是原子晶体
⑦分子晶体的熔点一定比金属晶体低
⑧NaCl晶体中,阴、阳离子的配位数都为6.
A. ①③④⑦ B. ②④⑥⑧ C. ③⑤⑦⑧ D. ③④⑥⑦
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2017届安徽省“江南十校”高三3月联考理综化学试卷(解析版) 题型:选择题
化学与生产和生活密切相关,下列有关说法正确的是
A. 刚玉硬度仅次于金刚石,熔点也相当高,刚玉坩埚可用于熔融KHSO4
B. CO2是大量使用的灭火剂,但着火的镁条在CO2中继续燃烧说明它也可以助燃
C. 人血清中的血浆铜蓝蛋白相对分子质量为151000,是人工合成的高分子化合物
D. 三氯化铁易形成水合晶体,加热Fe2O3·6H2O晶体,可获得纯净的FeC13
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江省哈尔滨市高二3月月考化学试卷(解析版) 题型:选择题
合成氨反应:N2(g)+3H2(g)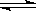 2NH3(g)△H=-92.4kJ•mol-1,在反应过程中,正反应速率的变化如图.下列说法正确的是( )
2NH3(g)△H=-92.4kJ•mol-1,在反应过程中,正反应速率的变化如图.下列说法正确的是( )
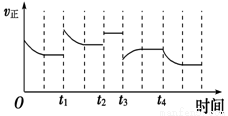
A. t1时升高了温度
B. t2时使用了催化剂
C. t3时增大了压强
D. t4时降低了温度
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省洛阳市高二(平行班)3月月考化学试卷(解析版) 题型:简答题
氟及氟产品在工农业生产中应用非常广泛,回答下列问题:
(1)基态氟原子核外电子的运动状态有__种,这些电子的电子云形状有__种;氟原子的外围电子排布式为______.
(2)NaHF2(氟化氢钠)电解可制氟气,NaHF2中所含作用力的类型有_____;与HF2-互为等电子体的分子有___(举一例).
(3)N2F2(二氟氮烯)分子中,氮原子的杂化轨道类型为____.
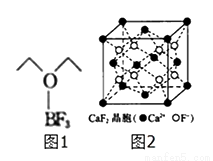
(4)三氟化硼乙醚(如图1)的熔点为-58℃,沸点为126~129℃,它属于__晶体.
(5)氟化钙的晶胞结构如图2所示,晶胞参数α=0.555nm.
①Ca2+、F-的配位数分别为__和__.
②列式表示氟化钙晶体的密度:_________g•cm-3(不必计算出结果).
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省洛阳市高二(平行班)3月月考化学试卷(解析版) 题型:选择题
下列描述中正确的是
A. ClO3-的空间构型为平面三角形
B. SiF4和 SO32-的中心原子均为 sp3杂化
C. 在所有的元素中,氟的第一电离能最大
D. C2H5OH 分子中共含有 8 个极性键,1 个 π 键
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省洛阳市高二(平行班)3月月考化学试卷(解析版) 题型:选择题
下列有关卤族元素及其化合物的表示正确的是( )
A. 氟离子的结构示意图: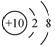 B. 次氯酸的结构式:H-Cl-O
B. 次氯酸的结构式:H-Cl-O
C. 溴化铵的电子式: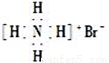 D. 质子数为53,中子数为78的碘原子:
D. 质子数为53,中子数为78的碘原子: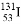
查看答案和解析>>
科目:高中化学 来源:2017届陕西省西安市高三模拟(一)理综化学试卷(解析版) 题型:选择题
如右图所示,甲池的总反应式为:N2H4+O2=N2+2H2O,下列关于该电池工作时的说法正确的是
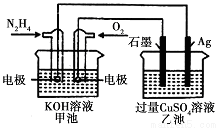
A. 该装置工作时,Ag电极上有气体生成
B. 甲池和乙池中的溶液的pH均减小
C. 甲池中负极反应为N2H4-4e-=N2+4H+
D. 当甲池中消耗0.1molN2H4时,乙池中理沦上最多产生6.4g固体
查看答案和解析>>
科目:高中化学 来源:2017届江苏省苏州市高三上学期期末考试化学试卷(解析版) 题型:简答题
“温室效应”是全球关注的环境问题之一。CO2是目前大气中含量最高的一种温室气体,CO2的综合利用是解决温室及能源问题的有效途径。
(1)研究表明CO2和H2在催化剂存在下可发生反应生成CH3OH。己知部分反应的热化学方程式如下:
CH3OH(g)+ O2(g) = CO2(g)+2H2O(1) △H1=akJ•mol-1
O2(g) = CO2(g)+2H2O(1) △H1=akJ•mol-1
H2(g)+ O2(g) = H2O(1) △H2=bkJ•mol-1
O2(g) = H2O(1) △H2=bkJ•mol-1
H2O(g) = H2O(l) △H3=ckJ•mol-1
则 CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=__________kJ•mol-1
CH3OH(g)+H2O(g) △H=__________kJ•mol-1
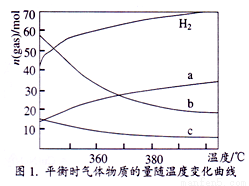
(2)CO2催化加氢也能合成低碳烯烃: 2CO2(g)+6H2(g) C2H4(g)+4 H2O (g),不同温度下平衡时的四种气态物质的物质的量如图1所示,曲线b表示的物质为_______________ (写化学式)。
C2H4(g)+4 H2O (g),不同温度下平衡时的四种气态物质的物质的量如图1所示,曲线b表示的物质为_______________ (写化学式)。
(3)CO2和H2在催化剂Cu/ZnO作用下可发生两个平行反应,分别生成CH3OH和CO。
反应 A:CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
反应B:CO2(g)+ H2(g) CO(g)+H2O(g)
CO(g)+H2O(g)
控制CO2和H2初始投料比为1∶3时,温度对CO2平衡转化率及甲醇和CO产率的影响如图2所示。
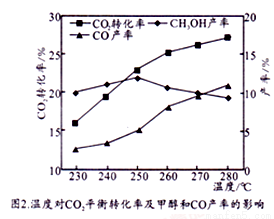
① 由图2可知温度升高CO的产率上升,其主要原因可能是__________________。
② 由图2可知获取CH3OH最适宜的温度是________________,下列措施有利于提高CO2转化为CH3OH的平衡转化率的措施有__________________。
A.使用催化剂 B.增大体系压强
C.增大CO2和H2的初始投料比 D.投料比不变和容器体积不变,增加反应物的浓度
(4)在催化剂表面通过施加电压可将溶解在水中的二氧化碳直接转化为乙醇,则生成乙醇的电极反应式为______________________________________________________。
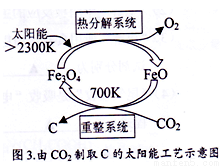
(5)由CO2制取C的太阳能工艺如图3所示。“热分解系统”发生的反应为:2Fe3O4 6FeO+O2↑ ,每分解1mol Fe3O4转移电子的物质的量为_____________;“重整系统”发生反应的化学方程式为_____________________________________________。
6FeO+O2↑ ,每分解1mol Fe3O4转移电子的物质的量为_____________;“重整系统”发生反应的化学方程式为_____________________________________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省扬州市高二下学期学业水平测试(二)化学试卷(解析版) 题型:选择题
下列实验装置、试剂选用及实验操作都正确的是
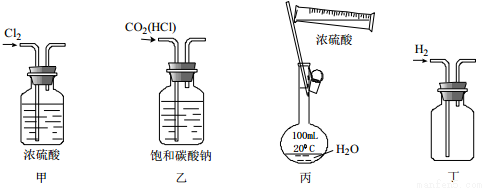
A. 用甲干燥Cl2 B. 用乙除去CO2中的HCl
C. 用丙配制一定浓度的H2SO4 D. 用丁收集一瓶H2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com